(12分)一定温度下,某容积为2 L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所示:
(1)该反应的化学方程式是 。
(2)在图上所示的三个时刻中, (填“t1”“t2”或“t3”)时刻处于平衡状态,此时v正 v逆(填“>”“<”或“=”);0- t2时间段内v(N)= 。
(3)已知M、N均为气体,若反应容器的容积不变,则“压强不再改变” (填“能”或“不能”)作为该反应已达到平衡状态的判断依据。
(4)已知M、N均为气体,则下列措施能增大反应速率的是 (选填字母)。
| A.升高温度 | B.降低压强 |
| C.减小M的浓度 | D.将反应容器体积缩小 |
已知某溶液中只存在OH-.H+.NH4+.Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种,请回答后面问题:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)上述关系一定不正确的是(填序号)
(2)若溶液中只有一种溶质,则该溶质为,该溶液中离子浓度的大小关系为(填序号)
(3)若关系③正确,则溶液中溶质为。
(4)若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显(填“酸性”、“碱性”、“中性”)。
(5)25℃,pH="a" 的盐酸VamL与pH=14-a的氨水VbmL混合,若溶液显中性,则VaVb(填>、<、=、无法确定)
元素A的单质能与H2化合生成HxA,在标准状况下8.5gHxA气体的体积是5.6L。含5.1g的HxA的溶液与200ml0.75mol/l的CuCl2溶液正好发生复分解反应,并生成黑色沉淀和一种强酸,则:
(1)A 元素的相对原子质量,若A 的质子数等于中子数,则A是元素(填名称)。
(2)A的最高价氧化物是(填化学式)。这一氧化物在室温下呈态,将其熔化需要克服。
(3)HxA与CuCl2溶液反应的离子方程式。
(4)A的单质在常温下是固体,在常温常压下0.25mol该单质完全燃烧放出QkJ的热量。写出该反应的热化学方程式:。
五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。
回答下列问题:
(1)五种元素中,原子半径最大的是,非金属性最强的是(填元素符号)。
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是(用化学式表示)。
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为,其中存在的化学键类型为。
(4)单质D在充足的单质E中燃烧,反应的化学方程式为;
(5)单质E与水反应的离子方程式。
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①将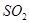 通入酸性
通入酸性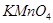 溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是。
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是。
| A.S2- | B.S | C.SO32- | D.SO42- |
②亚硫酸钠中的硫呈+4价,它既有氧化性又有还原性,现有试剂:溴水、H2S、稀硫酸。
请选取合适的试剂证明Na2SO3具有还原性, 并写出该反应的离子方程式为:.
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。其中属于碱性氧化物的是。
②现取一份蛇纹石试样进行实验:
I.先将其溶于过量的盐酸中、过滤,滤渣的主要成分是。
II.再向滤液中加入NaOH溶液至过量、过滤,滤渣中的主要成分是。
I.用元素符号回答原子序数11-18的元素的有关问题:(填对应物质的化学式)
(1)最高价氧化物的水化物碱性最强的是;其电子式为:
(2)最高价氧化物的水化物呈两性的是;
(3)能形成气态氢化物且最稳定的是,其电子式为.
II.化学是一门以实验为基础的自然科学,根据已有实验知识回答下列问题。
下列说法错误的是。
| A.将Cl2通入紫色石蕊试液,溶液先变红后褪色 |
| B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C.配制1L0.5mol·L-1的NaCl溶液,需用托盘天秤称量29.25gNaCl固体 |
| D.常温下,可以用铁质容器储运浓硝酸 |
E.实验室可以用加热氯化铵的方法制取少量氨气
F.实验室保存硫酸亚铁溶液,需在试剂瓶内加入铁粉或铁钉,防止硫酸亚铁被氧化
G.除去KCl溶液中少量MgCl2:加入适量NaOH溶液,过滤