下列指定反应的离子方程式正确的是
| A.向NaOH溶液中通入过量CO2:2OH-+CO2=CO32-+H2O |
B.电解氯化镁溶液:2Cl-+2H2O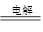 Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.向H2O2溶液中加入MnO2:2H2O2+4H++MnO2=O2↑+Mn2++4H2O |
| D.向KAl(SO4)2溶液中滴加Ba(OH)2溶液至SO42—沉淀完全:Al3++2SO42—+2Ba2++4OH—=AlO2-+2BaSO4↓+2H2O |
取5 mL 0.1 mol·L-1KI溶液,滴加0.1 mol·L-1FeCl3溶液5~6滴,继续加入2 mLCCl4,充分振荡,静置。下列有关该实验的说法不正确的是
| A.下层CCl4溶液呈紫红色 |
| B.取少量上层溶液,滴加酸性AgNO3溶液,若有黄色沉淀产生,则表明该反应存在化学反应限度 |
| C.取少量上层溶液,滴加KSCN溶液,若溶液显红色,则表明该反应存在化学反应限度 |
| D.该实验中KI与FeCl3反应后(未加CCl4),溶液中存在Fe3+、Fe2+、I—、I2等微粒 |
把下列四种碳酸氢钠溶液分别加入四个盛有10 mL 2 mol·L-1盐酸的烧杯中,均加水稀释到50 mL,此时碳酸氢钠和盐酸反应,其中反应开始时速率最大的是
| A.10 ℃ 20 mL 3 mol·L-1的碳酸氢钠溶液 |
| B.20 ℃ 20 mL 2 mol·L-1的碳酸氢钠溶液 |
| C.20 ℃ 20 mL 4 mol·L-1的碳酸氢钠溶液 |
| D.10 ℃ 20 mL 2 mol·L-1的碳酸氢钠溶液 |
已知可逆反应:2SO2(g)+O2(g) 2SO3(g)△H=-akJ·mol-1下列关于此反应的说法中错误的是
2SO3(g)△H=-akJ·mol-1下列关于此反应的说法中错误的是
| A.加压可使该反应的反应速率变大 |
| B.升高温度,该反应的正、逆反应速率均变大 |
| C.将2molSO2和1molO2混合进行反应,反应完成时放出的热量为akJ |
| D.单位时间内生成2molSO2,同时消耗1molO2说明该反应达到平衡状态 |
下列说法中正确的是
| A.离子化合物中可以含有共价键,但共价化合物中一定不含离子键 |
| B.含有共价键的物质一定是共价化合物 |
| C.HCl溶于水只需克服分子间作用力 |
| D.干冰升华时,分子内共价键会发生断裂 |
已知反应X + Y =" M" + N为吸热反应,对这个反应的下列说法中正确的是
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.X和Y的总能量一定低于M和N的总能量 |
| D.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |