某温度下,对于反应N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol。
2NH3(g) △H=-92.4kJ/mol。
N2的平衡转化率(α~%)与体系总压强(P)的关系如下图所示。下列说法正确的是: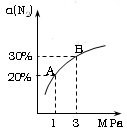
A.将1.0mol氮气、3.0mol氢气,置于1L密闭容器中发生反应,放出的热量为92.4kJ
B.平衡状态由A变到B时,平衡常数K(A) < K(B)
C.上述反应在达到平衡后,增大压强,H2的转化率提高
D.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
下列过程属于人工固氮的是
| A.分离液态空气制氮气 | B.闪电时N2转化为NO |
| C.工业合成氨 | D.豆科作物根瘤菌将N2转化为含氮化合物 |
下列做法不能体现低碳生活的是
| A.减少食物加工过程 | B.注意节约用电 |
| C.尽量购买本地的、当季的食物 | D.大量使用薪柴为燃料 |
若不小心误将水加入你家里的食用花生油里,你将采用下列何种方法分离
| A.过滤 | B.分液 | C.渗析 | D.萃取 |
根据我省中心气象台报道,近年每到春季,我省沿海一些城市多次出现大雾天气。根据物质的分类,雾属于下列分散系中的
| A.溶液 | B.悬浊液 | C.乳浊液 | D.胶体 |
实验是化学研究的一种重要手段,现有下图所示A~G七种仪器,请根据要求填空。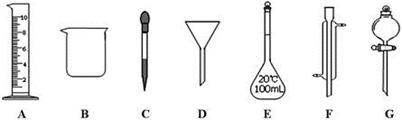
(1)写出仪器名称:E,F
(2)下列实验操作中用到仪器G的是(选填下列选项的编号字母)。
a.分离水和CC14的混合物
b.分离水和酒精的混合物
c.分离水和泥砂的混合物
(3)实验室配制100mL 0.5mol/L的盐酸溶液。
①下列关于仪器E的使用方法中,正确的是(选填下列选项的编号字母)。
a.使用前应检查是否漏液 b.使用前必须烘干
c.不能用作物质反应或溶解的容器 d.热溶液可直接转移到容量瓶中
②需要10mol/L的浓盐酸mL。取用该体积盐酸时,需要用到上述仪器中的A和(选填仪器的编号字母)。