常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
| A.HA为强酸 |
| B.该混合液pH=7 |
| C.图中X表示HA,Y表示OH-,Z表示H+ |
| D.该混合溶液中:c(A-)+ c(Y)=c(Na+) |
已知:相同温度下Ka(HF)﹥Ka(HCN)。现有物质的量浓度和体积均相同的NaF和NaCN两种溶液,已知前者溶液中所含离子数目为n1,后者溶液中所含离子数目为n2,下列关系正确的是
| A.溶液pH:NaF﹥NaCN | B.n1 ﹥n2 | C.n1 ﹤n2 | D.c(F-)﹤c(CN-) |
在由水电离产生的H+浓度为1×10-13 mol/L的溶液中,一定能大量共存的离子组是
①K+、Al3+、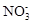 、S2-
、S2-
②K+、Fe2+、I-、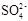
③Na+、Cl-、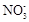 、
、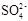
④Na+、Ca2+、Cl-、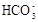
⑤K+、Ba2+、Cl-、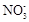
| A.①③ | B.③⑤ | C.③④ | D.②⑤ |
如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是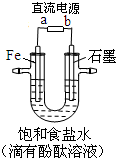
| A.a 为电源的正极 |
| B.通电一段时间后,石墨电极附近溶液先变红 |
| C.Fe电极的电极反应是4OH-- 4e-=2H2O+O2↑ |
D.电解饱和食盐水的总反应是: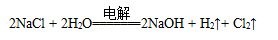 |
在FeCl3溶液中滴加无色的KSCN溶液后,有以下可逆反应存在:FeCl3+3KSCN  Fe(SCN)3 +3KCl。已知Fe(SCN)3呈红色,则在该平衡体系中加入少量KCl晶体后(忽略溶液体积的变化),红色将
Fe(SCN)3 +3KCl。已知Fe(SCN)3呈红色,则在该平衡体系中加入少量KCl晶体后(忽略溶液体积的变化),红色将
| A.变深 | B.变浅 | C.不变 | D.无法确定 |
等物质的量浓度的下列溶液中,c(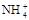 )最大的是
)最大的是
| A.NH4HCO3 | B.NH4NO3 | C.(NH4)2CO3 | D.NH4HSO4 |