某鱼雷采用Al-AgO动力电池,以溶解有氢氧化钾的流动海水为电解液,电池反应为:2Al+3AgO+2KOH=3Ag+2KAlO2+H2O,下列说法不正确的是
| A.AgO为电池的正极 | B.Al在电池反应中被氧化 |
| C.电子由AgO极经外电路流向Al极 | D.溶液中的OH-向Al极迁移 |
下列叙述正确的是
| A.煤、石油、天然气等是化石燃料 |
| B.氢氧化钡晶体与氯化铵晶体的反应是放热反应 |
| C.直接燃烧煤比将煤进行处理转化为气体或液体燃料再燃烧效果好 |
| D.酸与碱发生中和反应时放出的热量叫中和热 |
不符合原子核外电子排布基本规律的是
| A.核外电子总是优先排在能量最低的电子层上 |
| B.K层是能量最低的电子层 |
| C.N电子层为次外层时,最多可容纳的电子数为18 |
| D.各电子层(n)最多可容纳的电子数为n2 |
以下有关原子结构及元素周期律、元素周期表的叙述正确的是
| A.第IA族元素铯的两种同位素137Cs比133Cs多4个质子 |
| B.元素周期表有十八个纵行,共十六个族 |
| C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
| D.同主族元素从上到下,单质的熔点逐渐降低 |
为纪念编制了第一个元素周期表的俄国化学家门捷列夫,人们把第101号元素(人工合成元素)命名为钔。该元素最稳定的一种原子可以表示为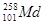 ,该原子所含中子的数目为
,该原子所含中子的数目为
| A.56 | B.157 | C.258 | D.101 |
在一密闭容器中有如下反应:aX(g)+bY(g) nW(g);ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
nW(g);ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图: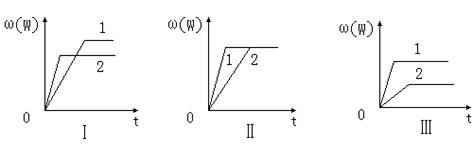
其中,ω(W)表示W在反应混合物中的体积分数,t表示反应时间。当其它条件不变时,下列分析正确的是
| A.图Ⅰ可能是不同压强对反应的影响,且p2>p1,a+b<n |
| B.图Ⅱ可能是不同压强对反应的影响,且p1>p2,n<a+b |
| C.图Ⅱ可能是在同温同压下催化剂对反应的影响,且1使用的催化剂效果好 |
| D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,ΔH<0 |