对下列图像的描述中,正确的是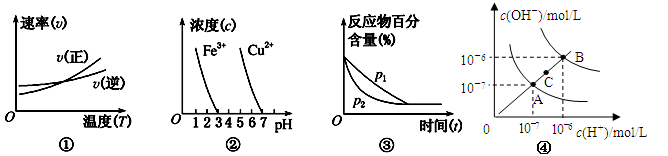
| A.根据图①可判断正反应的ΔH <0 |
| B.根据图②,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 |
C.图③可表示压强(p)对反应2A(g)+2B(g) 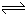 3C(g)+D(s)的影响 3C(g)+D(s)的影响 |
| D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
熔融碳酸盐燃料电池,是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔金属阳极、金属极板构成的燃料电池。其电解质是熔融态碳酸盐。下图是用熔融碳酸盐作电解质,氢气和氧气形成的燃料电池;下列说法正确的是: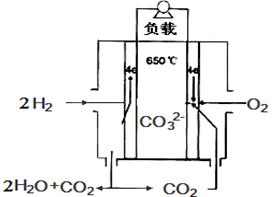
| A.该电池放电时,负极的反应式为:H2 - 2e-+CO2 =H2O+ CO32- |
| B.该电池中CO32-的为由左边移向右边移动 |
| C.该电池放电时,正极的反应式为:O2 +2CO2+ 4e- =2CO32- |
| D.该电池放电时,当转移4mol e-时正极消耗1mol O2和1mol CO2 |
相同温度下,在体积相等的三个密闭容器甲、乙、丙中发生可逆反应:N2(g)+ 3H2(g)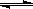 2NH3(g)△H=-92.4 kJ/mol。其中甲为恒温恒容容器,乙为恒温恒压容器、丙为恒容绝热容器;实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4 kJ/mol。其中甲为恒温恒容容器,乙为恒温恒压容器、丙为恒容绝热容器;实验测得起始、平衡时的有关数据如下表:
| 容器编号 |
起始时各物质物质的量/mol |
平衡时反应中的能量变化 |
||
| N2 |
H2 |
NH3 |
||
| ① |
1 |
3 |
0 |
放出热量a kJ |
| ② |
1 |
3 |
0 |
放出热量b kJ |
| ③ |
2 |
6 |
0 |
放出热量c kJ |
下列叙述正确的是
A.N2的转化率:丙是甲的二倍
B.三个容器内反应的平衡常数:甲=乙>丙
C.达平衡时氨气的体积分数:甲>乙>丙
D.放出热量关系: b < a < 92.4
某原电池装置如图所示。下列有关叙述中,正确的是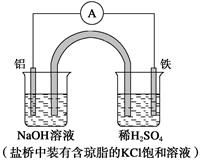
| A.Fe作正极,发生氧化反应 |
| B.负极反应:Al-3e-+3OH-===Al(OH)3↓ |
| C.工作一段时间后,盛有稀硫酸溶液的杯中pH不变 |
| D.盐桥中的Cl-向左边烧杯中移动,使该烧杯中溶液保持电中性 |
将1mol N2O5置于2L密闭容器中,在一定温度下发生下列反应:①2N2O5(g) 2N2O4(g)+O2(g); ②N2O4(g)
2N2O4(g)+O2(g); ②N2O4(g) 2NO2(g)。达到平衡时,c(O2)=0.2 mol·L-1,c(NO2)=0.6mol·L-1,则此温度下反应①的平衡常数为
2NO2(g)。达到平衡时,c(O2)=0.2 mol·L-1,c(NO2)=0.6mol·L-1,则此温度下反应①的平衡常数为
| A.3.2 | B.0.2 | C.1/180 | D.4/45 |
某同学按下图所示的装置进行试验。A、B为两种常见金属,它们的硫酸盐可溶于水。当K闭合时,在交换膜处SO42一从右向左移动。下列分析错误的是
A.金属活动性A强于B
B.反应初期,y电极的电极反应为:2Cl--2e-=Cl2↑
C.反应初期,x电极周围出现白色沉淀,后来电极附近沉淀溶解
D.电解一段时间后将AlCl3溶液倒入烧杯并搅拌可得到偏铝酸盐溶液