(每空2分,共12分)已知X、Y、Z、W、L为五种短周期元素,非金属元素X最外层电子数与其周期序数相同,Y的最外层电子数是其所在周期数的2倍。Y在Z中充分燃烧能生成其最高价化合物YZ2。W+与Z2-具有相同的电子数。X在L中燃烧,产物XL溶于水得到一种强酸。请回答下列问题:
(1)X在周期表中的位置是 。请写出实验室制备单质L的化学方程式 ,尾气处理的离子方程式: 。
(2)由X分别与Y、Z形成的最简单化合物的稳定性关系为: 。
(3)由X、Y、Z、W组成的一种盐,在面食中有大量使用,其俗名为: ,在其水溶液中滴入由X、Y、Z形成的日常生活中常见的一种酸,反应的离子方程式为: 。
H、D、T三种微粒,它们相互之间关系是,
同温同压下,它们单质的密度之比是,
在1mol单质中,它们的质子数之比是,
在相同状况下,1L单质中,它们的电子数之比是。
取少量Fe2O3粉末(红褐色)加入适量盐酸,化学反应方程式为:,得到棕黄色的FeCl3溶液,用此溶液分别做如下实验:在小烧杯中加入20 mL蒸馏水,煮沸后,滴入几滴FeCl3溶液,继续煮沸至溶液呈红褐色,即制得,用激光笔照射烧杯中的液体,可以观察到液体中出现,这个现象叫。
(1)同温同压下,某瓶充满氧气时质量为116g,充满二氧化碳时,质量为122g,充满气体A时质量为114g,A的摩尔质量为_______。
(2)8.4g N2与9.6g某单质Rx,所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是,x值为。
下列两个反应均为在溶液中进行的反应,试按下列要求作答:
①在表格中填出反应式中的氧化剂、还原剂,氧化产物、还原产物。
②将其改写成离子方程式;
(1) 2FeCl3 + H2S =2FeCl2 + S↓ + 2HCl
| 氧化剂: |
还原剂: |
||
| 氧化产物: |
还原产物: |
离子方程式为:____________________________________。
(2)MnO2 + 4HCl(浓) 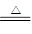 MnCl2 + 2H2O + Cl2↑
MnCl2 + 2H2O + Cl2↑
| 氧化剂: |
还原剂: |
||
| 氧化产物: |
还原产物: |
离子方程式为:___________________________________。
从①Ba(OH)2 ②HCl ③Zn ④CuSO4 ⑤CaCO3中选出合适的物质,实现下列各题要求的变化,写出化学反应的化学方程式,是离子反应的写出离子方程式。
(1)实验室制取CO2的反应
(2)实验室制取H2的反应
(3)生成沉淀的反应
(4)盐与金属的置换反应
(5)酸碱之间的中和反应