化学与生产、生活密切相关,下列说法正确的是
| A.焰火的五彩缤纷是某些金属元素化学性质的展现 |
| B.将煤气化后再作为能源,可减少PM2.5引起的危害 |
| C.用激光笔分到照射盛有蓝墨水、FeCl3溶液的玻璃杯均出现光亮的通路 |
| D.氨气液化时能吸收大量的热,常用来做冷冻剂 |
下列有关化学用语使用正确的是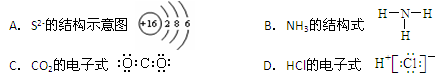
从如图所示的某气体反应的能量变化分析,以下判断错误的是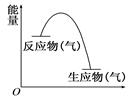
| A.这是一个放热反应 | B.该反应可能需要加热 |
| C.生成物的总能量低于反应物的总能量 | D.反应物比生成物更稳定 |
下表为部分短周期元素的原子半径及主要化合价的有关信息,以下叙述正确的是
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
| 主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2 |
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
已知氯元素天然存在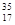 Cl、
Cl、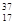 Cl两种同位素,若知氯元素的相对原子质量为35.5,则
Cl两种同位素,若知氯元素的相对原子质量为35.5,则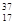 Cl所占的原子百分比是
Cl所占的原子百分比是
| A.25% | B.75% | C.50% | D.80% |
有六种微粒,它们分别是: 、
、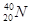 、
、 、
、 +、
+、 2+、
2+、 -,它们所属元素的种类为
-,它们所属元素的种类为
| A.3种 | B.4种 | C.5种 | D.6种 |