碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”.实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量NaC1,加热到一定温度,持续通入SO2,待反应一定时间,过滤得到粗碲.
(1)反应的总化学方程式为:TeOSO4+2SO2+3X Te↓+3H2SO4,则X为 (化学式).
Te↓+3H2SO4,则X为 (化学式).
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaC1浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
| 实验 |
温度/℃ |
反应时间/h |
粗蹄沉淀率 |
| a |
65 |
3.0 |
65.0 |
| b |
80 |
3.0 |
98.9 |
| c |
80 |
2.0 |
98.9 |
| d |
90 |
2.0 |
97.0 |
①该小组研究的反应条件是 和 .
②实验a和b的目的是 .
③在上述四组实验中,最佳的反应条件是 ℃和 h.
④为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率.若再设计对比实验,选择的反应条件还可以是 (填选项).
A.80℃,1.5h B.80℃,2.5h
C.70℃,2.0h D.95℃,2.0h.
(一)如图所示,把试管放入盛有25 ℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入 5 mL 盐酸于试管中.
试回答下列问题:
(1)实验中观察到的现象是
(2)产生上述现象的原因是
(3)写出有关反应的离子方程式:
(4)由实验推知,MgCl2溶液和H2的总能量 (填“大于”“小于”或“等于”)镁片和盐酸的总能量。
(二)某实验小组用0.50 mol·L- 1 NaOH溶液和0.50mol·L- 1 的硫酸溶液进行中和热的测定,实验装置如图所示: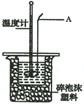
(1)仪器A的名称为 ;
(2)装置中碎泡沫塑料的作用是 ;
(3)写出该反应中和热的热化学方程式: (中和热为57.3 kJ·mol- 1) ;
亚硝酸钠被称为工业盐,不能用作食品工业,但在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略)。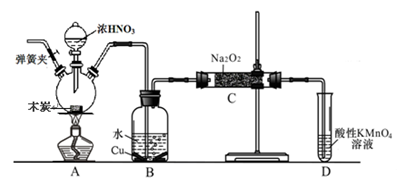
已知:室温下,①2NO+Na2O2 = 2NaNO2
②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式 。
(2)B中观察到的主要现象是有无色气体产生和 ,D装置的作用是 。
(3)检验C中产物有亚硝酸钠的方法是 。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物应在B、C装置间增加装置,则该装置中盛放的药品名称 。
(5)将7.8g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g。
亚硝酸钠常用作食品防腐剂。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸的反应及生成气体产物的成分。
已知:①NO+NO2+2OH-===2NO2-+H2O
②气体液化的温度:NO2:21℃、NO:-152℃
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(按左→右连接):
(2)组装好仪器后,接下来进行的操作是 .
(3)关闭弹簧夹K1,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体中含有NO,依据的现象是___________________。
②装置B的作用是____________________,装置E的作用是______________
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为 。如果没有装置C,对实验结论造成的影响是_________________________。
下表是实验室制备气体的有关内容:
| 编号 |
实验内容 |
实验原理 |
气体发生装置 |
| ① |
制备氧气 |
H2O2→O2 |
|
| ② |
制备氨气 |
NH4Cl→NH3 |
|
| ③ |
制备氯气 |
HCl→Cl2 |
(1) 从上述气体制备原理中:从制备过程看,必须选择合适的氧化剂才能实现的是 (填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是 。
(2) 根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中。
ⅠⅡ Ⅲ Ⅳ
(3) 某学习小组设计了如下图实验,将氯气依次通过下列装置以验证氯气的性质: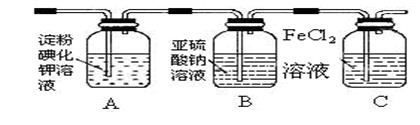
①通入氯气后,A中的现象是 ,整套实验装置存在的明显缺陷是 。
②C装置中发生反应的离子方程式为: 。
(1)用5.0mol﹒L-1的NaOH溶液配制0.1mol﹒L-1的NaOH溶液时,如图所示的仪器中,肯定不需要的是 (填序号),配制上述溶液还需要的玻璃仪器是 (填仪器名称)。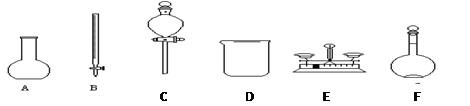
(2)在配制过程中,下列操作将导致所配溶液浓度偏低的是(填编号)



 ①准确取出的浓NaOH溶液在空气中露置时间过长;
①准确取出的浓NaOH溶液在空气中露置时间过长; ②用量器将浓NaOH溶液直接加入容量瓶,缓慢加入蒸馏水至液面最低点恰好和环形刻度线相切;
②用量器将浓NaOH溶液直接加入容量瓶,缓慢加入蒸馏水至液面最低点恰好和环形刻度线相切;
③摇匀后,液面低于刻度线,再加蒸馏水至液面最低点恰好和环形刻度线相切;
④稀释NaOH溶液的仪器未洗涤。