下列我国古代的技术应用中,其工作原理不涉及化学反应的是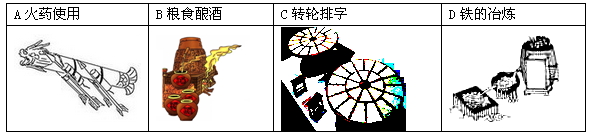
下列每组物质中含有化学键类型相同的是( )
| A.NaCl、HCl、H2O、NaOH | B.Cl2、Na2S、HCl、SO2 |
| C.HBr、CO2、H2O、CS2 | D.Na2O2、H2O2、H2O、O3 |
下列电子式或结构式错误的是( )
下列化合物中阳离子与阴离子的半径比最小的是()
| A.KI | B.LiF | C.LiI | D.KF |
已知短周期元素的离子aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A.原子半径: A>B>D>C | B.原子序数: d>c>b>a |
| C.离子半径:C2->D->B+>A2+ | D.单质的还原性: A>B>D>C |
X、Y、Z是周期表中相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31,则X、Y、Z分别是( )
| A.Mg、Al、Si | B.Li、Be、Mg | C.N、O、S | D.P、S、O |