aX(g)+bY(g)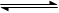 cZ(g)+dW(g)在一定体积的密闭容器中反应5 min达到平衡时,X减少n mol·L-1,Y减少
cZ(g)+dW(g)在一定体积的密闭容器中反应5 min达到平衡时,X减少n mol·L-1,Y减少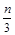 mol·L-1,Z增加
mol·L-1,Z增加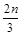 mol·L-1。若将体系压强增大,W的百分含量不发生变化。则化学方程式中各物质的化学计量数之比a∶b∶c∶d应为
mol·L-1。若将体系压强增大,W的百分含量不发生变化。则化学方程式中各物质的化学计量数之比a∶b∶c∶d应为
| A.3∶1∶2∶1 | B.1∶3∶2∶2 |
| C.3∶1∶2∶2 | D.1∶3∶1∶2 |
近年来,冠以“绿色”的新概念不断产生,如绿色食品、绿色材料、绿色能源、绿色化学等,这里的“绿色”是对人类社会可持续发展战略的形象表述。“绿色化学”要求以经济、环保和技术上设计可行的化学反应。据此,由单质镁制造硝酸镁的下列四个方案中,你认为可行而且符合“绿色化学”要求的方案是()
A.Mg Mg(NO3)2 Mg(NO3)2 |
B.Mg MgCl2 MgCl2 Mg(OH)2 Mg(OH)2 Mg(NO3)2 Mg(NO3)2 |
C.Mg MgO MgO Mg(NO3)2 Mg(NO3)2 |
D.Mg MgSO4 MgSO4 Mg(NO3)2 Mg(NO3)2 |
下列叙述错误的是()
| A.原子半径:Cl>S>O | B.还原性:Na>Mg>Al |
| C.稳定性:HF>HCl>HBr | D.酸性:HClO4>H2SO4>H3PO4 |
在①硫酸②重晶石③三氧化硫④绿矾四种化合物中,硫元素的质量分数由高到底排列的顺序是()
| A.①>②>③>④ | B.②>③>④>① |
| C.①>③>②>④ | D.③>①>②>④ |
下列除去杂质的操作方法正确的是()
| A.NO中有少量的NO2:用水洗涤后再干燥 |
| B.食盐中有少量的NH4Cl:加过量的烧碱溶液后加热蒸干 |
| C.N2中有少量的O2:通过灼热的氧化铜 |
| D.硝酸钾中的少量氯化钠:溶解,低温蒸发结晶,洗涤,干燥 |
某金属氧化物化学式为R2O3,相对分子质量为102,电子数为50,已知氧原子核内有8个中子,R原子核内中子数是()
| A.27 | B.13 | C.21 | D.14 |