下列实验操作、现象和原因解释不合理的是
| 选项 |
实验操作 |
实验现象 |
原因解释 |
| A. |
将一片较簿的铝片放在酒精灯火焰上灼烧 |
铝片慢慢熔化呈液滴状 |
铝表面的氧化膜致密且熔点很高,阻碍铝与氧气的接触,同时铝的熔点较低熔化了 |
| B. |
将等表面积的镁条、铝片(均除去氧化膜)分别放入装有等浓度、等体积盐酸的两支试管中 |
都产生气泡,镁条表面产生气泡更快 |
镁的金属性比铝的金属性强,镁更易失去电子,所以反应更快 |
| C. |
在打磨过的铁片上先滴一滴饱和食盐水,再滴一滴酚酞 |
液滴的外圈先出现红色 |
铁片不纯含有碳元素,铁、碳与食盐水形成原电池,溶液外圈发生吸氧腐蚀,导致c(OH-)增大,溶液呈碱性 |
| D. |
取少量淀粉加稀硫酸,加热几分钟,冷却后加入新制氢氧化铜悬浊液,加热至沸腾 |
未见砖红色沉淀生成 |
淀粉水解后没有葡萄糖生成 |
不粘锅内壁涂有一薄层聚四氟乙烯涂层,聚四氟乙烯商品名为“特氟隆”。下列关于聚四氟乙烯的说法中,正确的是( )
| A.聚四氟乙烯的单体是不饱和烃 |
| B.聚四氟乙烯能够承受高温而不发生任何变化 |
| C.聚四氟乙烯中氟元素的质量分数为76% |
| D.聚四氟乙烯的化学活泼性较大 |
下列物质不属于复合非金属材料的是( )
| A.碳化硅纤维 | B.生物陶瓷 |
| C.钢化玻璃 | D.氮化硅陶瓷 |
一种可降解塑料为PBS,它的名称叫聚乙烯琥珀酸,结构式为:
它的性能优越,而且废弃后一旦回收入土,几个月就可完全分解。下列关于PBS的说法中不正确的是( )
| A.PBS的熔点为62 ℃,耐热性能优异,沸水以下、冰点以上都可以使用 |
| B.纯PBS制品价格较贵,在生产中适当填充一些无机填料或天然大分子的复合物如淀粉等,既能降低价格,又不影响其性能及降解 |
| C.PBS在使用时仍然具有与其他塑料相同的性能,如耐腐蚀、强度大、密度小、绝缘性好等 |
| D.PBS属于加聚反应的产物,能在酸性或碱性条件下水解 |
聚乳酸(PLA)是一种常用的可降解塑料,它的熔点为175 ℃,被加工成薄膜或纤维,有比较好的耐水分解性。这种塑料还有促进植物生长的作用,因此可用它制作植物移植或植物栽培用容器等;通过压轧,它还可以被制成透明的、机械性能良好的纤维、薄膜、容器和镜片等。下列关于PLA说法中正确的是(双选)( )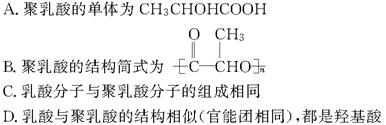
下列有关新型有机高分子材料的说法中,不正确的是( )
| A.高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工、酿造业等 |
| B.复合材料一般是以一种材料作基体,另一种材料作增强剂 |
| C.导电塑料是应用于电子工业的一种新型有机高分子材料 |
| D.合成高分子材料制成的人工器官都受到人体的排斥作用,难以达到生物相容的程度 |