2014年5月7日南京某建设公司丢失用于材料探伤的放射源Ir—192(铱—192)一枚,经相关部门的努力追查,丢失的放射源于5月10日被回收,Ir—192的放射性会对人体产生很大的伤害。已知Ir元素位于周期表中第6周期第Ⅷ族,原子序数为77,192为该核素的质量数,下列关于Ir—192的说法正确的是
| A.Ir—192核外含有115个电子 |
| B.Ir为非金属元素 |
| C.Ir—192中子数与质子数的差为38 |
| D.Ir元素与碘元素位于同一周期 |
下列实验设计能够成功的是()
| 实验目的 |
实验操作 |
|
| A |
实验室制备硝基苯 |
将苯和浓硝酸混合后加热 |
| B |
除去硫酸钠溶液中少量氯化钠杂质 |
向含有氯化钠杂质的硫酸钠溶液中加入适量的硝酸银溶液,过滤 |
| C |
检验溴乙烷发生消去反应的产物 |
向盛有少量溴乙烷的试管中,先加入氢氧化钠溶液,加热,再滴人用硝酸酸化 的硝酸银溶液 的硝酸银溶液 |
| D |
浓硝酸的氧化性强于稀硝酸 |
向盛有少量的浓硝酸、稀硝酸的两支试管中,分别加入大小相同的铜片 |
X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如图3所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是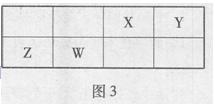 ()
()
| A.Y元素最高价氧化物对应的水化物化学式为H3YO4 |
| B.原子半径由小到大的顺序为:X<Z<Y<W |
| C.与同浓度的盐酸反应,Z比W更剧烈 |
| D.X、Z两种元素的氧化物中所含化学键类型相同 |
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为:
CH3CH2OH—2e—====X+2H+。下列说法中正确的是()
| A.电池内部H+由正极向负极移动 |
| B.另一极的电极反应式为:O2+4e—+2H2O===4OH— |
| C.乙醇在正极发生反应,电子经过外电路流向负极 |
D.电池总反应为:2CH3CH2 OH+O2→2CH3CHO+2H2O OH+O2→2CH3CHO+2H2O |
常温下,若HA溶液和NaOH溶液混合后pH =7,下列说法不合理的是()
| A.反应后HA溶液可能有剩余 |
B.生成 物NaA的水溶液的pH可能小于7 物NaA的水溶液的pH可能小于7 |
| C.HA溶液和NaOH溶液的体积可能不相等 |
| D.HA溶液的c(H+)和NaOH溶液的c(OH—)可能不相等 |
用NA表示阿伏加德罗常数,下列说法正确的是()
| A.0.2 mol H2O:完全分解转移的电子数为0.4NA |
| B.300 mL 2 mol/L蔗糖溶液中所含分子数为0.6NA |
| C.在标准状况下,2.8 g N2和2.8 g CO所含电子数均为1.4NA |
| D.在常温常压下,2.24 L SO2与O2混合气体中所含氧原子数为0.2NA |