常温下,下列关于电解质溶液的说法正确的是
| A.将pH=4的CH3COOH溶液加水稀释10倍,溶液中各离子浓度均减小 |
| B.用CH3COOH溶液滴定等物质的量浓度的NaOH溶液至pH=7,V(CH3COOH溶液)<V(NaOH溶液) |
| C.向0.2 mol/L的盐酸溶液中加入等体积0.1 mol·L-1 NH3·H2O溶液:c(Cl–)+c(OH–)=c(H+)+c(NH3·H2O) |
| D.在含0.1mol NaHSO4的溶液中:c(H+)=c(SO42-)+c(OH–) |
下列各实验中,先产生沉淀,然后沉淀又溶解的是()
①向饱和碳酸钠溶液中通入CO2至过量
②向氯化铝溶液中逐滴加入氢氧化钠溶液至过量
③向AgNO3溶液中逐滴加入氨水至过量
④向硅酸钠溶液中逐滴加入盐酸至过量
| A.①② | B.①③ | C.①④ | D.②③ |
在25℃时,将a mol/L的醋酸溶液与0.01mol/L氢氧化钠溶液等体积混合,充分反应后溶液呈中性。下列说法不正确的是()
| A.a一定大于0.01 |
| B.反应后溶液中一定有c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| C.反应后溶液中一定有c(CH3COO-)+c(CH3COOH)>c(Na+) |
| D.反应后溶液中一定有c(Na+)>c(CH3COO-)>c(H+)=c(OH) |
已知下列热化学方程式: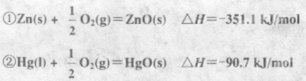
由此可知Zn(s)+HgO(s)=ZnO(s)+Hg(l)的反应热△H为
| A.+260.4kJ/mol | B.-260.4kJ/mol | C.-441.8kJ/mol | D.+441.8kJ/mol |
下列除去杂质的方法中,正确的是()
| A.除去铜粉中混有的铁粉:加足量稀硝酸,过滤 |
| B.除去N2中少量的CO2:通过足量灼热的CuO粉末 |
| C.除去CO2中的少量的HCl:通过足量的饱和碳酸氢钠溶液 |
| D.除去KCl溶液中的少量CaCl2:加适量Na2CO3溶液,过滤 |
设NA表示阿伏加德罗常数的数值,下列叙述正确的是()
| A.0.25mol Na2O2中含有的阴离子数为0.5N0 |
| B.1mol α- 氨基乙酸(甘氨酸)分子中存在10N0对共用电子 |
| C.标准状况下,2.24L CHCl3含有的分子数为0.1N0 |
| D.足量铜与1L 18mol·L-1浓硫酸反应可以得到SO2的分子总数为9N0 |