氯化钠是氯碱工业的主要原料,其晶体不带有结晶水,饱和食盐水也是实验室常用试剂。完成下列填空:
(1)粗盐中含有Ca2+、Mg2+、SO42―等离子和少量泥沙,某同学设计的提纯步骤依次为:溶解、过滤、加入沉淀剂、调pH、蒸发结晶。其中还缺少的步骤是_________。
(2)电解饱和食盐水实验中,检验阳极产物的试剂是________________;若用粗盐配制饱和食盐水进行电解,则阴极区可能出现的异常现象是_________________。
(3)氯碱厂称固体烧碱为“片碱”。用滴定法测定片碱中杂质Na2CO3含量的过程如下:
称取样品,加水溶解;加入酚酞试液,用标准盐酸滴定至溶液由红色刚好变为无色;再加甲基橙,继续用标准盐酸滴定至终点。数据处理。实验中用于溶解片碱的蒸馏水必须事先煮沸一段时间,煮沸的目的是_______;用甲基橙作指示剂时,判断滴定达到终点的现象是________________;用酚酞作指示剂时,发生反应的离子方程式为_________________。
(4)下列关于饱和食盐水的用途及装置设计正确的是_________(填写编号)。

a.模拟工业制纯碱 b.制乙酸乙酯实验中接受产物
c.除去氯气中的氯化氢 d.实验室制乙炔
(5)在饱和食盐水中加入浓硫酸,会有大量固体析出。过滤、洗涤、得干燥固体。为确定该固体的成份,进行以下实验:①取少量固体溶于水,测得溶液显中性;
②称取1.961 g固体于坩埚中加热,发现有水生成,继续加热至固体恒重,称量质量为1.331 g。判断固体已恒重的操作是____________________;
③将1.331 g固体全部溶于水,加入足量的BaCl2溶液,得干燥纯净沉淀1.165 g。则原固体的成份是______________(写化学式)。
紫杉醇是一种新型抗癌药,其分子式为C47H51NO14,它是由如下的A酸和B醇生成的一种酯。
B.R—OH(R是一个含C、H、O的基团)
(1)A可在无机酸催化下水解,其反应方程式是___________________________________。
(2)A水解所得的氨基酸不是天然蛋白质水解产物,因为氨基不在(填希腊字母)_______位。
(3)写出ROH的分子式:____________。
(12分)如图所示进行乙醇的催化氧化实验,试管A中盛有无水乙醇,玻璃管B中装有CuO(用石棉绒作载体)。请回答下列问题:
(1)向试管A中鼓入空气的目的是___________________________________________。
(2)试管A上部放置铜丝的作用是___________________________________________。
(3)玻璃管中可观察到的现象是_____________________________________;相关化学方程式是____________________________________________________________________。
(4)试管C中放的是蒸馏水,在实验过程中试管C导管口有气泡冒出,从液面逸出的气体的主要成分是__________________。
(6分)中国在新工业化发展过程中,开发可再生能源以缓解石油短缺引起的能源危机是一个重要的课题。2003年元月份,辽宁省投资建设一个年产工业酒精500万吨的工厂,目的是为了将工业酒精与汽油混合作为汽车燃料而减少汽油的消耗量。已知制酒精的方法有三种:
方法一:在催化剂作用下乙烯与水反应
方法二:CH3-CH2Br + H2O CH3CH2OH + HBr
CH3CH2OH + HBr
方法三:(C6H10O5)n(淀粉)+nH2O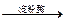 nC6H12O6(葡萄糖)
nC6H12O6(葡萄糖)
C6H12O6(葡萄糖)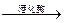 2C2H5OH + 2CO2↑
2C2H5OH + 2CO2↑
(1)你认为应用哪一种方法生产工业酒精能够缓解石油短缺带来的能源危机?为什么?
(2)方法一的化学反应方程式是:_________________________________________________。
(3)乙醇燃烧的化学方程式是:__________________________________________________。
(12分)已知葡萄糖在乳酸菌的催化作用下,可以生成乳酸,其分子式是C3H6O3。
(1)写出葡萄糖转化为乳酸的化学方程式:__________________________________________。
(2)无色透明的乳酸溶液能使紫色石蕊溶液变红色;能够在加热、浓硫酸作催化剂的条件下与乙酸进行酯化反应,则
①乳酸中含有的官能团的符号和名称是:____________________________。
②若乳酸中还含有一个甲基(—CH3),则乳酸的结构简式为___________________________。
(3)写出下列化学方程式:
①钠与乳酸的反应:____________________________________________________________。
②乳酸与乙酸的酯化反应:______________________________________________________。
(9分)同学们已经学习了几种典型的有机化学反应类型——取代反应、加成反应、酯化反应,写出下列反应的化学反应方程式,并判断其反应类型。
(1)由乙烯制氯乙烷:____________________________,属于______________反应。
(2)由苯制取硝基苯:____________________________,属于______________反应。
(3)由苯制取环己烷:____________________________,属于______________反应。