【2015新课标Ⅱ卷理综化学】原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同。下列叙述错误的是
| A.元素的非金属性次序为c>b>a |
| B.a和其他3种元素均能形成共价化合物 |
| C.d和其他3种元素均能形成离子化合物 |
| D.元素a 、b、c各自最高和最低化合价的代数和分别为0、4、6 |
下列混合溶液中,各离子浓度的大小顺序正确的是()
A.10mL0.1mol·L-1氨水与10mL0.1mol·L-1盐酸混合:c(Cl-)>c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
| B.10mL0.1mol·L-1NH4Cl溶液与5mL0.2mol·L-1NaOH溶液混合:c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| C.10mL0.1mol·L-1CH3COOH溶液与5mL0.2mol·L-1NaOH溶液混合:c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
| D.10mL0.5mol·L-1CH3COONa溶液与6mL1mol·L-1盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
常温下pH=2的一元弱酸HA溶液,其电离百分率为5%,0.01mol·L-1的一元碱BOH溶液中,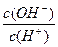 =1×1010。将上述两种溶液等体积混合后,得到溶液中各离子浓度大小关系正确的是()
=1×1010。将上述两种溶液等体积混合后,得到溶液中各离子浓度大小关系正确的是()
| A.c(OH-)>c(H+)>c(B+)>c(A-) | B.c(B+)=c(A-)>c(H+)>c(OH-) |
| C.c(B+)>c(A-)>c(H+)>c(OH-) | D.c(A-)>c(B+)>c(H+)>c(OH-) |
常温下将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是()
| A.pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-) |
| B.pH>7,且c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| C.pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| D.pH=7,且c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
下列操作,能使电离平衡H2O H++OH-向右移动,且溶液呈酸性的是()
H++OH-向右移动,且溶液呈酸性的是()
| A.向水中加入NaHSO4溶液 | B.向水中加入Al2(SO4)3溶液 |
| C.向水中加入Na2CO3溶液 | D.将水加热到100℃,使pH=6 |
把Ca(OH)2放入蒸馏水中,一定时间后达到如下平衡:Ca(OH)2(s) Ca2++2OH-,向其中加入少量下列溶液可使Ca(OH)2减少的是()
Ca2++2OH-,向其中加入少量下列溶液可使Ca(OH)2减少的是()
| A.Na2S溶液 | B.AlCl3溶液 |
| C.NaOH溶液 | D.CaCl2溶液 |