【2015新课标Ⅱ卷理综化学】甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
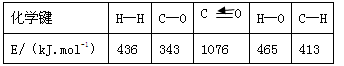
由此计算△H1= kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3= kJ·mol-1。
(2)反应①的化学平衡常数K的表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是 。
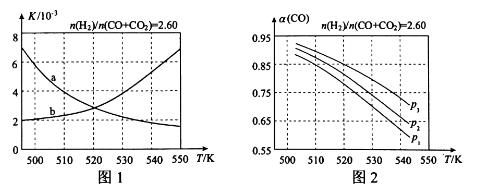
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而 (填“增大”或“减小”),其原因是 。图2中的压强由大到小为_____,其判断理由是_____。
有几种元素的微粒的电子层结构如图所示,其中:
(1)某原子微粒性质很稳定,一般不和其他元素的原子反应,这种微粒符是____________;
(2)某微粒的盐溶液,加入AgNO3溶液时会出现白色沉淀,这种微粒符号______________;
(3)某原子失去一个电子得到该微粒,则这种微粒的符号是____________________;
(4)某原子得到两个电子得到该微粒,则这种微粒的符号是____________________。
将下列硅酸盐改写成氧化物的形式(aMxOy•bSiO2•cH20)。
①镁橄榄石(Mg2SiO4)_________________________________;
②高岭石Al2Si2O9 H4____________________________________。
选择合适的序号填空
A.12C、13C、14CB.S2-、Cl—、Na+
C.金刚石、石墨、C60D.Na+、Ne、F-
属于同素异形体的是,同位素的是,最外层电子数相同的微粒是,电子层数相同的微粒是,化学性质基本相同的是。
选择合适的序号填空
| A.氢氧化铝 | B.二氧化硅 | C.硅 | D.铝热剂 E.铝合金 |
可广泛做为半导体的是,用于净水的是,可做光导纤维的是,用于焊接钢轨的,具有抗腐蚀性强、密度小、强度高等优点的是。
E是某类化妆品生产的常用添加剂(香料),工业上以Y、X为主要原料合成,其中Y的产量可以用来衡量一个国家石油化工发展水平产品,其流程图如下。请完成填空:
(1) 已知A、B的相对分子质量相差16,则A结构简式为_
(2) 写出反应⑤的化学反应方程式
(3)E(乙酸苯甲酯)有多种同分异构体,其中属于酯类、且为一取代苯结构的有
种(不包括E本身),任写其中一种的结构简式。
(4)除图示方法外,请你另设计一种最佳方案由Y制得A(用类似以上流程图表示)
(5)若将反应③、④的条件做如下变动,将先后得到 、
、 而得不到
而得不到 、
、 :
:
已知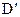 与
与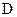 的分子式相同,且
的分子式相同,且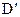 可与
可与 溶液发生显色反应,写出符合条件的由X→
溶液发生显色反应,写出符合条件的由X→ (
( 的一硝基代物有2种)的反应方程式_______。
的一硝基代物有2种)的反应方程式_______。