【2015浙江理综化学】下列说法正确的是
| A.为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 |
| B.做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸。如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 |
| C.在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42-或SO32- |
| D.提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 |
下图是向100mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图像。根据图像所得结论正确的是( )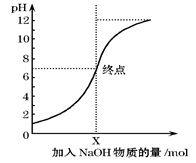
| A.原来盐酸的物质的量浓度为1mol·L-1 |
| B.X为0.1mol·L-1的NaOH溶液 |
| C.原来盐酸的物质的量浓度为0.1mol·L-1 |
| D.X为0.01mol·L-1的NaOH溶液 |
0.1mol·L-1盐酸滴定0.1mol·L-1NaOH溶液,如达到滴定终点时不慎多加了1滴盐酸(1滴溶液体积约为0.05mL),继续加水至50mL,所得溶液的pH是( )
| A.4 | B.7.2 | C.10 | D.11.3 |
在-50℃时,液氨的电离跟水的电离相似,存在平衡,2NH3(l) NH4++NH2—,NH4+的平衡浓度为1×10-15mol·L-1,下列说法错误的是( )
NH4++NH2—,NH4+的平衡浓度为1×10-15mol·L-1,下列说法错误的是( )
| A.在液氨中加入NaNH2,可使液氨的离子积变大 |
| B.在液氨中加入NH4Cl,液氨的离子积不变 |
| C.此温度下液氨的离子积K为1×10-30 |
| D.在液氨中加入金属钠可能有NaNH2生成 |
在相同温度下,100mL 0.1mol·L-1的醋酸与10mL 1mol·L-1的醋酸相比较,下列说法正确的是( )
| A.发生中和反应时所需NaOH的量前者大于后者 |
| B.前者的电离程度小于后者 |
| C.所含H+的物质的量前者大于后者 |
| D.所含CH3COOH的物质的量前者大于后者 |
下列叙述正确的是( )
| A.碳酸钙难溶于水,放入水中溶液不导电,且碳酸钙在960℃时分解,不存在熔融状态导电的性质,故CaCO3是非电解质 |
| B.SO3溶于水后得到的水溶液导电,故SO3是电解质 |
| C.BaSO4在水中溶解度很小,但溶解部分全部电离,故BaSO4是强电解质 |
| D.H3PO4晶体在熔融状态下和溶于水后都能导电,故H3PO4强是电解质 |