下表列出了部分元素的原予结构示意图。下列叙述不正确的是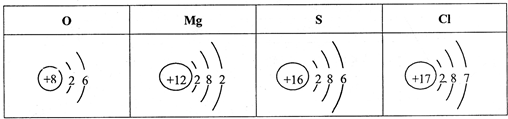
| A.硫原子在化学反应中易得到电子 |
| B.O2-的核外电子总数为10 |
| C.由镁元素和硫元素组成化合物的化学式为Mg2S |
| D.氧元素和硫元素化学性质具有相似性的原因是它们的原子最外层的电子数相同 |
下列叙述与胶体性质无关的是 ( )
| A.同一支钢笔使用不同品牌墨水时,容易发生堵塞现象 |
| B.当日光从窗隙射入灰尘飞扬的房间时,可观察到一束光线 |
| C.明矾具有净水作用 |
| D.向氯化铁溶液中加入氢氧化钠溶液,产生红褐色沉淀 |
在某溶液中酚酞呈粉红色。下列离子在该溶液中不能大量存在的是 ()
| A.K+ | B.Na+ | C.Al3+ | D.Ba2+ |
配制250mL0.10mol·L-1的NaOH溶液时,下列实验操作会使配得的溶液浓度偏大是( )
| A.转移溶液后未洗涤烧杯和玻璃棒就直接定容 |
| B.NaOH固体溶解后立即转入容量瓶 |
| C.在容量瓶中进行定容时仰视刻度线 |
| D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度 |
下列说法中,正确的是:()
| A.为加快过滤速度,可用玻璃棒在过滤器中搅拌 |
| B.胶体、溶液、浊液分属不同类别的本质是其透过滤纸的性质不同 |
| C.分液漏斗和容量瓶使用前都需要检查是否漏液 |
| D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
下列说法正确的是(NA表示阿伏加德罗常数的值)()
| A.28 g氮气所含有的原子数目为NA |
| B.在常温常压下,11.2 L N2含有的分子数为0.5 NA |
| C.0.5 mol单质铝与足量盐酸反应转移电子数为1.5NA |
| D.标准状况下,1 L水所含分子数为1/22.4NA |