除去下列各物质中混有的少量杂质(括号内为杂质),所用除杂试剂及操作方法均正确的是
| 选项 |
物质 |
试剂 |
操作方法 |
| A |
CO2(CO) |
O2 |
点燃 |
| B |
NaCl溶液(Na2SO4) |
Ba(NO3)2溶液 |
先加入适量Ba(NO3)2,溶液后过滤 |
| C |
CaO(CaCO3) |
稀盐酸 |
滴加适量稀盐酸 |
| D |
Cu(Fe) |
稀硫酸 |
先加入适量稀硫酸,再过滤、洗涤、干燥 |
下列有关化学用语或名称表达正确的是
A.亚硫酸的电离方程式:H2SO3 2H++SO32- 2H++SO32- |
B.乙炔的分子结构模型示意图: |
C.H2O2的电子式: |
D. 的名称3-甲基-1-丁醇 的名称3-甲基-1-丁醇 |
化学与新型材料、环境保护、能源开发等密切相关。下列说法错误的是
| A.人造纤维、合成橡胶和光导纤维都属于有机高分子化合物 |
| B.使用生物酶降解生活废水中的有机物,可防止水体的富营养化 |
| C.上海世博会很多展馆采用光电转化装置,体现当今“低碳”经济的理念 |
| D.利用二氧化碳等原料合成聚碳酸酯类可降解塑料,有利于减少白色污染 |
某pH=1的X溶液中可能含有Fe2+、A13+、NH4+、CO32―、SO32―、SO42―、C1―中的若干种,现取X溶液进行连续实验,实验过程及产物如下: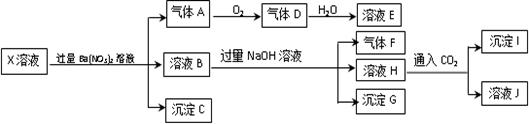
下列说法正确的是
| A.气体A是NO2 |
| B.X中肯定存在Fe2+、A13+、NH4+、SO42- |
| C.溶液E和气体F不能发生化学反应 |
| D.X中不能确定的离子是 A13+和C1- |
将CH4设计成燃料电池,其利用率更高,装置示意如图(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL。则下列说法错误的是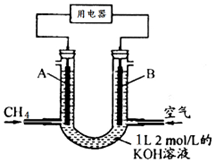
A.通入CH4的一端为原电池的负极,通入空气的一端为原电池的正极
B.0<V≤22.4L时,电池总反应的化学方程式为:CH4+2O2+2KOH=K2CO3+3H2O
C.22.4L<V≤44.8L时,负极电极反应为:CH4-8e-+9CO32- +3H2O=10HCO3-
D.V=33.6L时,溶液中阴离子浓度大小关系为: c(CO32- )>c(HCO3- )>c(OH-)
下列关于①乙烯;②苯;③乙醇;④乙酸;⑤葡萄糖等有机物的叙述不正确的是
| A.可以用新制的Cu(OH)2悬浊液鉴别③④⑤ |
| B.只有①③⑤能使酸性KMnO4溶液褪色 |
| C.只有②③④能发生取代反应 |
| D.一定条件下,⑤可以转化为③ |