下图为某化学反应的速率与时间的关系示意图。下列有关t1时刻改变条件的说法正确的是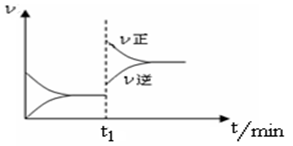
A.2SO2(g)+O2(g)  2SO3(g) ΔH<0,t1时刻升高温度 2SO3(g) ΔH<0,t1时刻升高温度 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2浓度 4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2浓度 |
C.H2O(g)+CO(g)  H2(g)+CO2(g) ΔH>0, t1时刻增大压强 H2(g)+CO2(g) ΔH>0, t1时刻增大压强 |
D.C(s)+H2O(g) CO(g)+H2(g) ΔH>0,t1时刻升高温度 CO(g)+H2(g) ΔH>0,t1时刻升高温度 |
铜粉放入稀硫酸溶液中,加热后无明显现象发生。当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出。该盐是()
| A.Fe2(SO4)3 | B.Na2CO3 | C.KNO3 | D.FeSO4 |
取一干燥烧瓶,用排空气法收集氨气,做喷泉实验。当水充满约整个烧瓶容积的二分之一后,喷泉停止,烧瓶内的氨水的物质的量浓度是()
| A.0.045mol•L-1 | B.1mol•L-1 | C.0.029mol•L-1 | D.不能确定 |
38.4g铜跟一定量的浓硝酸反应,铜全部作用后共收集到混合气体22.4L(标准状况下),反应消耗的硝酸的物质的量为()
| A.1mol | B.1.6 mol | C.2.2 mol | D.2.4 mol |
下列离子方程式书写正确的是
| A.将过量的NaOH溶液滴入同浓度的少量Ca(HCO3)2溶液中 Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| B.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全 Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C.向Ca(ClO)2溶液中通入适量SO2 Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| D.向FeI2溶液中加少量氯水:2Fe2++Cl2=2Fe3++2Cl- |
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是()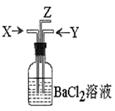
| A.洗气瓶中产生的沉淀是碳酸钡 | B.Z导管出来的气体中无二氧化碳 |
| C.气瓶中产生的沉淀是硫酸钡 | D.Z导管口有无色气体出现 |