下列反应的离子方程式正确的是
| A.向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O = Fe(OH)3↓+3H+ |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
D.用Pt电极电解饱和氯化镁溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
下列说法正确的是(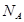 代表阿伏加德罗常数值)
代表阿伏加德罗常数值)
A.1molNa被完全氧化为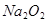 ,失去的电子数为2 ,失去的电子数为2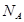 |
B.常温常压下,16g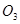 气体含有氧原子数为 气体含有氧原子数为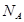 |
C.常温常压下,22.4LCO2含有的分子数为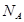 |
D.18gD2O所含的电子数为10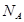 |
解析下列事实的离子方程式不正确的是
A.氨水使湿润的红色石蕊试纸变蓝:NH3·H2O NH4++OH- NH4++OH- |
| B.工业上用过量的溶液吸收SO2:SO2+OH-=HSO3- |
| C.用烧碱溶液清洗铝表面的氧化膜:2OH-+Al2O3=2AlO2-+H2O |
| D.用石灰乳吸收泄漏的氯气:Ca(OH)2+Cl2=Ca2++Cl-+ClO-+H2O |
六氯丙烷(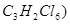 的同分异构体有
的同分异构体有
| A.2种 | B.3种 | C.4种 | D.5种 |
下列有关说法中,正确的是
| A.苯和乙烯都可以使溴的四氯化碳溶液褪色 |
| B.等物质的量的乙烯和乙醇完全燃烧消耗氧气的量不相等 |
| C.乙醇的酯化反应和酯的水解反应均属于取代反应 |
| D.聚乙烯可以发生加成反应 |
下列实验装置设计正确且能达到目的的是
| A.实验I:静置一段时间,小试管内有晶体析出 |
| B.实验II:制取氧气 |
| C.实验III除CO2气体中的HCL |
| D.实验IV:配制一定物质的量浓度的稀硫酸 |