设NA代表阿伏加德罗常数的数值,下列说法正确的是
| A.1 mol硫酸铝钾中阴离子所带电荷总数为2NA |
| B.等质量的乙炔和苯分别完全燃烧,乙炔和苯都消耗7.5 NA个氧气分子 |
| C.将0.1 mol碳酸钠溶于1 L水中,所得溶液含有CO32-和HCO3-共0.1 NA个 |
| D.在H2O2作燃料电池的负极原料时,每摩尔H2O2转移的电子数为2 NA |
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( )
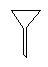

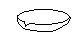
| A.蒸馏、过滤、萃取、蒸发 | B.蒸馏、蒸发、萃取、过滤 |
| C.萃取、过滤、蒸馏、蒸发 | D.过滤、蒸发、萃取、蒸馏 |
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是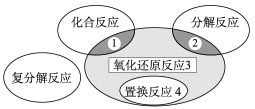
| A.2H2+O2点燃2H2O | B.CuO+CO 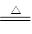 Cu + CO2 Cu + CO2 |
C.2NaHCO3 Na2CO3+H2O +CO2↑ Na2CO3+H2O +CO2↑ |
D.Zn +H2SO4 =ZnSO4 + H2↑ |
下列电离方程式书写正确的是()
| A.H2SO4 ="==" 2H+ + S6+ + 4O2- | B.Al2(SO4)3 ="==" 3Al3+ + 2SO42- |
| C.Ba(NO3)2 ="==" Ba2++ 2(NO3)2- | D.Ba(OH)2 ="==" Ba2+ + 2 OH- |
下列实验操作中,错误的是()
| A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B.蒸馏时,应使温度计水银球位于蒸馏烧瓶支管处 |
| C.用酒精萃取碘水溶液中的碘 |
| D.称量时将称量物放在称量纸或烧杯中,置于托盘天平的左盘,砝码放在托盘天平的右盘中 |
NaH与水反应的化学方程式为NaH+H2O==NaOH+H2↑,在该反应中NaH()
| A.是氧化剂 | B.是还原剂 |
| C.既是氧化剂又是还原剂 | D.既不是氧化剂又不是还原剂 |