(14分)已知A、B、C、D、E、F、G为七种短周期的主族元素,原子序数依次增大。已知:A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、G在元素周期表中处于相邻位置,这三种元素最外层电子数之和为17,质子数之和为31。D与F同周期,且在该周期中D元素的原子半径最大(稀有气体除外)。根据以上信息回答下列问题:
(1)B、C、G的氢化物中稳定性最强的是______(填化学式),沸点最高的是______ (填化学式)。
(2)D、E、F形成的简单离子半径由大到小的顺序为____________(用离子符号表示)。
(3)A与B能形成离子化合物BA5,该物质能与水剧烈反应生成一种气体和一种碱,则该反应的化学方程式为______________
(4)D的碳酸氢盐溶液与稀硫酸混合,当生成11.2L(标准状况)气体(不考虑气体溶解)时放热6.32kJ,写出该反应的热化学离子方程式_______________。
(5)科学家猜想宇宙中某星球上可能会存在着一种由A,B两种元素组成的一系列化合物,如BA3、B2A4、B3A5、B4A6等,该系列化合物的通式为_______(用元素符号表示)。有B2A4与另外两种等物质的量的该系列中的化合物组成的混合蒸气,在足量氧气中充分燃烧,只生成B元素的单质和水,且B元素的单质和水的物质的量之比为1:2,则另外两种化合物是______ (写化学式)。
现正开始使用一种安全气袋以防止汽车撞车时在驾驶室的人因向前冲撞发生意外。这种气袋内装有一种能在高温下分解出气体的混合物。例如有一种配方为:
61%—68%NaN3(叠氮化钠)、0%—5%NaNO3、0%—5%陶土、23%—28%Fe2O3粉、1%—2%SiO2粉、2%—6%石墨纤维。这些粉末经加压成型后,装在一个大袋子里,袋子放在驾驶室座位前。撞车时,约在10毫秒(10-3秒)内引发下列反应: 2NaN3=2Na+3N2(365℃分解)反应在约30毫秒内完成,袋内充满N2气而胀大,阻止人体前冲。在以后的100~200毫秒内气体“ 消失”,所以不致使人反弹,同时袋内的钠变成氧化钠。
消失”,所以不致使人反弹,同时袋内的钠变成氧化钠。
(1)你认为完成上述引发分解、生成气体的“消失”、钠变成氧化钠过程各需上述配方 里哪些物质和起什么作用。
里哪些物质和起什么作用。
(2)若气袋内放300g NaN3,在充满氮气时,袋内气体体积为(1大气压,300K)L 。若袋内气体压力达到4大气压(此时为350K),则袋内气体体积为L。
(3)配方中Fe2O3的量是如何控制的。
(4)叠氮离子中有三个氮原子连成直线,N—N键等长(116pm)。写出其电子式。
(5)怎样做到既使混合物在30毫秒内迅速分解,但又不燃烧、爆炸。
将固体CaC2O4·H2O放在一个可称量的容器中加热灼烧,固体质量随温度的升高而变化,测得数据如下:
| 温度/℃ |
25 |
325 |
700 |
1160 |
固体质量/ g g |
1.460 |
1.280 |
1.000 |
0.560 |
根据计算推理,完成下列填空:
(1)写出325℃和700℃时固体产物的化学式:、。
(2)写出325℃ ~ 700℃时发生的化学反应方程式:。
(3)计算出1160℃时,反应所得产物的摩尔质量:。
工业合成氨的反应N2+3H2= 2NH3的能量变化如下图所示,请回答有关问题: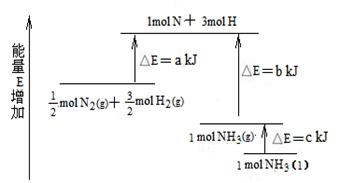
(1).合成 1 mol NH3(l) ____________(填“吸收”、“放出”)_____________kJ的热量。
(2).已知:拆开 lmol H—H 键、lmol N-H 键、lmol N≡N 键分别需要的能量是436kJ、391kJ、946kJ。则上图中的a=_______________kJ;1 mol N2(g) 完全反应生成NH3(g)产生的能量变化为 ______KJ。
(3).推测反应 2NH3(l)= N2(g)+3H2(g) 比反应 2NH3 (g)= N2(g)+3H2(g)______________(填“吸收”、“放出”)的热量_____________(填“多”、“少”)。
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。请回答下列问题:
(1)Y 元素的名称______________;
(2)W 在元素周期表中的位置是第____________周期第____________族;
(3)X2M2中存在的化学键有_______________________;
(4)Z、W氢化物的稳定性顺序为__________________;
(5)用电子式表示X2Z 的形成过程____________________________。
A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为 ,C为 (写元素符号)。
(2)写出A、B的化合物与E反应的化学方程式:
。
(3)A、B两元素形成化合物属(“离子”或“共价”)化合物。
(4)写出D的最高价氧化物的水化物和A反应的化学方程式:
。