甲、乙、丙、丁四种物质分别含两种或三种元素,它们的分子中各含l8个电子。甲是气态氢化物,在水中分步电离出两种阴离子。下列推断合理的是
A.某钠盐溶液含甲电离出的阴离子,则该溶液只能与酸反应
B.丁和甲中各元素质量比相同,则丁中一定含有-l价的元素
C.丙中含有第二周期ⅣA族的元素,则丙一定是只含C、H的化合物
D.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键
下列物质在常温下是气体的是( )
| A.甲醇 | B.甲醛 | C.四氯化碳 | D.乙醛 |
下列实验能获得成功的是( )
| A.将乙醛滴入银氨溶液中,直接加热煮沸制银镜 |
| B.苯与浓溴水反应制取溴苯 |
| C.向苯酚中加浓溴水观察沉淀 |
| D.1 mol·L—1 CuSO4溶液2 mL和0.5 mol·L—1 NaOH溶液2 mL混合后加入40%的乙醛溶液0.5 mL,加热煮沸观察沉淀的颜色 |
下列关于醛的说法不正确的是( )
| A.甲醛是甲基跟醛基相连而构成的醛 |
| B.醛的官能团是—CHO |
| C.甲醛和丙醛互为同系物 |
| D.饱和一元脂肪醛的通式为CnH2nO(n≥1) |
下列叙述正确的是( )
| A.苯中的少量苯酚可先加适量的浓溴水,再过滤而除去 |
| B.将苯酚晶体放入少量水中,加热时全部溶解,冷却后形成乳浊液 |
| C.苯酚的酸性很弱,不能使酸碱指示剂变色,但可以和NaHCO3反应放出CO2 |
| D.苯酚有毒,但其稀溶液可直接用作防腐剂和消毒剂 |
双酚A作为食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害很大。下列有关双酚A的叙述不正确的是( )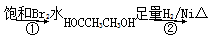
| A.双酚A的分子式是C15H16O2 |
| B.双酚A的核磁共振氢谱显示氢原子数之比是1∶2∶2∶3 |
| C.反应①中,1 mol双酚A最多消耗2 mol Br2 |
| D.反应②的产物中只有一种官能团 |