短周期元素的离子aW2+、bX+、cY2-、dZ-具有相同的电子层结构,下列推断正确的是
| A.原子半径:W>X>Z>Y | B.热稳定性:H2Y>HZ |
| C.离子半径:W2+>Y2- | D.碱性:XOH>W(OH)2 |
下列离子方程式书写不正确的是
A.用NaOH溶液吸收Cl2: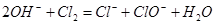 |
B.用浓盐酸与MnO2制取Cl2: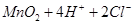 △ △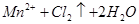 |
C.NaHCO3溶液与NaOH溶液反应: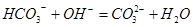 |
D.碳酸钙溶于醋酸溶液: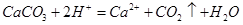 |
反应产物除与反应物的结构、性质有关,还与反应的条件有关。下列各组物质反应时:
①Cu与HNO3溶液②Cu与FeCl3溶液③Na与O2中,由于浓度或条件不同得到不同产物的是:
| A.①② | B.②③ | C.①③ | D.①②③ |
下列关于有机物的说法正确的是
| A.石油分馏和煤的干馏都是物理变化 |
| B.用溴水可以将甲烷和乙烯区分开 |
| C.“春蚕到死丝方尽”中“丝”的主要成分是纤维素 |
| D.淀粉和蛋白质完全水解的产物都是葡萄糖 |
下列说法中,不正确的是
| A.光导纤维的主要成分是SiO2 |
| B.大量排放SO2会引起酸雨 |
| C.明矾和漂白粉均可用于自来水的杀菌、消毒 |
| D.玻璃和陶瓷都属于传统硅酸盐材料 |
下列有关溶液中粒子浓度的关系式中,正确的是
A.pH相同的①CH3COONa、②NaHCO3、③C6H5ONa三份溶液中的c(Na+):③>②>①
B.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C.下图中pH=7时: c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
D.下图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)