甲、乙、丙、丁都是短周期元素,其中甲、丁在周期表中的相对位置如下表,甲原子最外层电子数是其内层电子数的2倍,乙单质在空气中燃烧发出黄色火焰,丙是地壳中含量最高的金属元素。下列判断正确的是
| A.简单离子半径:乙>丁 |
| B.乙与氧元素形成的某化合物中可能既有离子键,又有共价键 |
| C.乙、丙、丁三种元素最高价氧化物的水化物两两之间能发生反应 |
| D.甲与丁的核外电子数相差8 |
下列离子方程式书写正确的是
| A.将少量SO2气体通入NaClO溶液中 SO2+2ClO-+H2O=SO32-+2HClO |
| B.向KHSO4溶液中加入Ba(OH)2溶液至所得溶液的pH=7 Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| C.向Ca(HCO3)2溶液中滴入过量的NaOH溶液 Ca2++2 HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| D.112mL(S.T.P)Cl2通入10mL1mol/L的FeBr2溶液中 |
2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2
下列离子方程式的书写正确的是
| A.FeS固体与稀HNO3溶液混合 FeS+2H+=2Fe2++H2S↑ |
| B.NH4HSO4溶液中加入足量Ba(OH)2溶液 H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| C.Ca(ClO)2溶液中通入足量的CO2气体 Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
| D.等浓度等体积的Ca(H2PO4)2溶液与NaOH溶液混合 |
Ca2++H2PO4-+OH-=CaHPO4↓+H2O
下列离子方程式正确的是
| A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液,至沉淀完全: 2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| B.碳酸钠与醋酸溶液反应:CO32-+2CH3COOH=CO2↑+2CH3COO- +H2O |
| C.将1~2mL氯化铁饱和溶液加入到20 mL沸水中: Fe3++3H2O 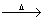 Fe(OH)3(胶体)+3H+ Fe(OH)3(胶体)+3H+ |
| D.氢氧化铁与氢碘酸中和:Fe(OH)3+3H+=Fe3++3H2O |
下列离子方程式正确的是
| A.AlCl3溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+; |
B.C6H5ONa溶液中通入少量CO2:2C6H5O-+CO2+H2O 2C6H5OH+ CO32-; 2C6H5OH+ CO32-; |
| C.FeBr2溶液中通入少量Cl2:2Br-+Cl2=Br2+2Cl-; |
| D.Mg(HCO3)2溶液中加入足量NaOH溶液: |
Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O.
下列各组离子,能够在溶液中大量共存的是:
| A.Na+、Al3+、NO3-、AlO2- | B.Na+、Ca2+、HCO3-、HSO4- |
| C.Cu2+、K+、NO3-、OH- | D.S2O32-、Na+、H+、SO42- |
E.Fe3+、Cl-、SCN-、K+ F.Fe3+、NH4+、Cl-、NO3-
G.Fe2+、Cl-、NO3-、H+ H.Na+、Al3+、SO42-、HCO3-