现有KCl和KBr的混合物3.87 g,将混合物全部溶于水,并加入过量的AgNO3溶液,充分反应后产生6.63 g沉淀物,则原混合物中钾元素的质量分数为
| A.24.1% | B.25.9% | C.40.3% | D.48.1% |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,0.05 mol·L-1 Fe2(SO4)3溶液中含Fe3+数目为0.1NA |
| B.标准状况下,22.4 L甲苯中含C-H数目为8 NA |
| C.常温下,9.2 g NO2和N2O4的混合气体中含有的氮原子数目为0.2 NA |
| D.1 mol氯气和足量NaOH溶液反应转移的电子数目为2NA |
下列装置进行相应的实验,能达到实验目的的是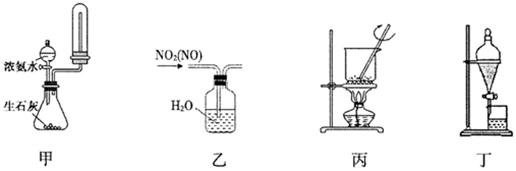
| A.用装置甲制取并收集干燥纯净的NH3 |
| B.用装置乙除去NO2中的少量NO |
| C.用装置丙将海带灼烧成灰 |
| D.用装置丁分离乙酸乙酯和饱和碳酸钠溶液 |
下列物质性质与应用对应关系正确的是
| A.漂白粉在空气中不稳定,可用于漂白纸张 |
| B.医用酒精能使蛋白质变性,可用于消毒杀菌 |
| C.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 |
| D.铜的金属活泼性比铁的弱,可在铁闸上装若干铜块以减缓其腐蚀 |
25℃时,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1mol·L-1 AlC13溶液中:H+、Na+、Cl-、SO42- |
| B.含有0.1mol·L-1 Fe3+的溶液中:Na+、K+、SCN-、NO3- |
| C.使甲基橙变红色的溶液中:Fe2+、K+、NO3-、SO42- |
| D.由水电离产生的c(H+)=10-12 mol·L-1的溶液中:NH4+、SO42-、HCO3-、Cl- |
下列有关化学用语表示正确的是
A.核内有8个中子的碳原子: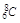 |
B.甲烷分子的比例模型: |
C.羟基的电子式: |
D.氯离子的结构示意图: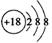 |