室温下,用0.100 mol·L-1 NaOH溶液分别滴定20.00ml 0.100 mol·L-1的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是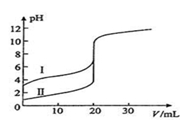
| A.II表示的是滴定醋酸的曲线 |
| B.pH=7时,滴定醋酸消耗V(NaOH)小于20ml |
| C.V(NaOH) =20.00ml时,两份溶液中c(Cl—)=c(CH3COO—) |
| D.V(NaOH) =10.00ml时,醋酸溶液中:c(Na+)>c(CH3COO—)>c(H+)>c(OH—) |
pH=2的两种一元酸X和Y,体积均为100 mL,稀释过程中pH与溶液体积的关系如下图所示。分别滴加NaOH溶液(c="0.1" mol·L-1)至pH=7,消耗NaOH溶液的体积为Vx、Vy,则()
| A.x为弱酸,Vx<Vy |
| B.x为强酸,Vx>Vy |
| C.y为弱酸,Vx<Vy |
| D.y为强酸,Vx>Vy |
已知:25℃时, Ksp[Mg(OH)2] = 5.61×10-12、Ksp [MgF2]=7.42×101。下列说法正确的是( )
| A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者c(Mg2+)大 |
| B.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 |
| C.25℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1NH4Cl溶液中的Ksp小 |
| D.25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化成MgF2 |
配制FeCl3溶液时,为防止其水解,应向溶液中加入少量
| A.HCl | B.H2O | C.NaCl | D.NaOH |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是()
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH+O2=CH3COOH+H2O |
| D.正极上发生的反应是:O2+4e-+2H2O=4OH- |