下列离子方程式中,正确的是
| A.大理石溶解于醋酸 CaCO3 + 2H+ ="=" Ca2+ + CO2↑+ H2O |
| B.澄清石灰水中加入CuSO4溶液混合 2OH- + Cu2+ ="=" Cu(OH)2↓ |
| C.NaHSO4溶液和Na2CO3溶液混合 2H++CO32-==CO2↑+ H2O |
| D.NaHSO4溶液中加入Ba(OH)2 Ba2+ + SO42- ="=" BaSO4↓ |
下列指定反应的离子方程式正确的是
A.NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH-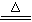 NH3↑+ H2O NH3↑+ H2O |
| B.NaHCO3溶液与氢氧化钠溶液反应:HCO3-+2OH-═CO2↑+H2O |
| C.用CH3COOH 溶液CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ |
| D.向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
决定化学反应速率的主要因素是
| A.反应物的浓度 | B.反应温度 | C.使用催化剂 | D.反应物的性质 |
球墨铸铁中含有一种铁碳化合物X。实验室测定化合物X的组成实验如下:
下列说法不正确的是
| A.固体2是氧化铁 |
| B.X的化学式可以表示为Fe3C2 |
| C.溶液甲中可能含有Fe3+ |
| D.X与足量的热浓硝酸反应有NO2和CO2生成 |
碘盐中添加的碘酸钾在工业上可用电解KI溶液制取,电极材料是石墨和不锈钢,化学方程式是:KI+3H2O KIO3+3H2↑,有关说法不正确的是
KIO3+3H2↑,有关说法不正确的是
| A.石墨作阳极,不锈钢作阴极 |
| B.I-在阳极放电,H+在阴极放电 |
| C.电解过程中电解质溶液的pH变小 |
| D.电解转移3 mol e-时,理论上可制得KIO3 107 g |
为实现下列实验目的,所用试剂合理的是
| 选项 |
实验目的 |
试剂 |
| A |
验证Br2的氧化性强于I2 |
溴水、KI溶液、淀粉溶液 |
| B |
除去Fe2O3中的Al2O3 |
稀盐酸 |
| C |
检验Fe3O4溶于盐酸后的金属阳离子 |
NaOH溶液 |
| D |
制备Fe(OH)3胶体 |
饱和FeCl3溶液、NaOH溶液 |