某小组欲用4.9%的稀
测一瓶标签破损的
溶液的质量分数.

(1)从一瓶标签模糊的
溶液里取出几滴后向
(2)取
溶液样品,并与4.9%的稀硫酸溶液混合.由图可得,完全反应时,所用稀硫酸溶液中溶质的质量为
(3)求
溶液样品中溶质的质量分数
某环保小组监测到一工厂排放的废水中含有H2SO4和CuSO4 。为了测定废水中CuSO4的质量分数,该小组取了100g废水,逐滴加入10%的NaOH溶液至过量。测得生成Cu(OH)2沉淀质量与所加NaOH溶液质量关系如下图所示。 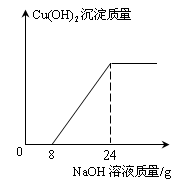
(1)与H2SO4反应的NaOH溶液质量为g;100g废水中H2SO4的质量为g。
(2)计算废水中CuSO4的质量分数。
某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
| 稀硫酸用量 |
剩余固体质量 |
稀硫酸用量 |
剩余固体质量 |
| 第一次加入10g |
mg |
第四次加入10g |
1.0g |
| 第二次加入10g |
2.0g |
第五次加入10g |
0.6g |
| 第三次加入10g |
1.5g |
第六次加入10g |
0.6g |
(1)从以上数据可知,这六次实验中,第次加入稀硫酸时样品中的镁已经完全反应;表格中,m=。
(2)第六次实验后,所得溶液中硫酸镁的质量分数(要求写出计算过程,结果保留到0.1%)
医学上常用双氧水来清洗创口和局部抗菌。小美同学为了测定一瓶医用双氧水溶液的溶质质量分数,取该双氧水69g放入烧杯中,然后加入2g二氧化锰,完全反应后,称得烧杯内剩余物质的总质量为69.4g。请回答下列问题;
(1)二氧化锰在反应中的作用是。
(2)该双氧水溶液的溶质质量分数(结果精确到0.1%)。
实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀
质量的关系曲线如图所示。
回答下列问题:
(1)从图中看出生成沉淀的最大质量是 g。
(2)开始加入碳酸钠溶液至10g时,还没有沉淀的原
因是 。
(3)计算原滤液中氯化钙的质量分数。
某长期暴露在空气中的烧碱样品已部分变质,为了测定其纯度,现进行如下实验:取样品18.6g加入到85.8g水中充分搅拌至完全溶解,向所得溶液中逐滴滴加稀盐酸,产生气体的质量与所加稀盐酸质量的关系如图所示。分析题意并回答下列问题: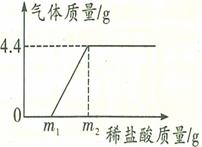
(1)反应过程中生成气体的质量是。
(2)该烧碱样品中氢氧化钠的质量是多少克(写出规范的解题过程)?
(3)所用稀盐酸的溶质质量分数是(用ml和m2表示)。