如图所示,甲、乙、丙、丁、戊分别是碳酸钠溶液、氧化铁、氢氧化钙溶液、氯化钡溶液和稀盐酸中的一种。图中短线相连的物质能相互发生反应。已知丙溶液能使紫色石蕊溶液变成红色。
请回答下列问题:

(1)丁物质的化学式是。
(2)甲与乙反应的化学方程式是。
(3)丙与戊反应的化学方程式是。
(4)向盛有甲溶液的烧杯中滴加丙溶液,烧杯中溶液的
会(填"增大"或"减小")。
甲、乙、丙、丁分别是石蕊溶液、稀硫酸、碳酸钠溶液、澄清石灰水中的一种,若用四个圆表示四种溶液,两圆相交部分为两溶液混合后出现的主要实验现象,如下图所示。请回答:
(1)丁是;通常其用途为。
(2)甲和丙的化学反应方程式为;反应类型为。
为了将混有硫酸钠、碳酸氢铵(不稳定,受热易分解生成氨气、二氧化碳和水)的氯化钠提纯,某同学设计的实验流程如图: :
:
试回答下列问题:
(1)操作①的目的是。操作②能否用硝酸钡溶液?(填“能”或“否”)。
(2)进行操作②后,如何判断SO42-已除尽,方法是。
(3)写出操作③有关的化学反应方程式。操作④的名称是。
(4)此设计方案是否严密,说明理由。
(5)原固体样品中含NaCl m1g,最后得到的NaCl固体m2g,则m1m2(填“>”、“<”或“=”)。
某粗盐(主要成分是NaCl)样品中含有少量沙土、CaCl2和MgCl2杂质。以下是除去粗盐样品中杂质的实验流程,根据此流程图回答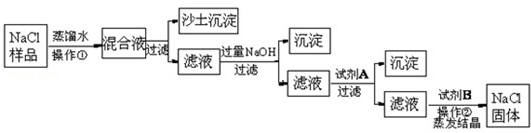
(1)操作①的名称是。
(2)加入NaOH目的是与滤液中MgCl2反应从而除去杂质。写出NaOH与MgCl2反应的化学方程式。
(3)加入试剂A的目的是与滤液中的CaCl2反应.则加入试剂A后,沉淀是。
(4)本实验多次采用过滤操作,如图是过滤装置.过滤时,液体沿玻璃棒慢慢向漏斗中倾倒,注意液面始终要边缘。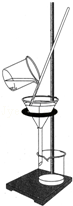
(5)操作②蒸发结晶时用到的玻璃棒的作用是。
A、B、C、D、E、F 都是初中化学中常见的化合物,其中B是酸,E、F是碱,它们之间可发生如下反应:①A+B→C+D②E+B→C+D③C+F→E↓(红褐色)+NaCl
根据上述信息回答问题:
(1)写出有关物质的化学式:A;E。
(2)写出下列反应的化学方程式:
反应①;
反应③。
通过海水晒制可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质。以下是制备精盐的实验方案: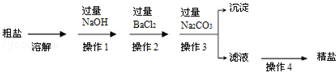
回答下列问题:
(1)操作1中,加入NaOH溶液除杂时,反应的化学方程式为;。
(2)操作2中,不能用硝酸钡溶液代替BaCl2溶液,原因是。
(3)加入Na2CO3除去的杂质离子是。
(4)进行操作3后,判断Na2CO3过量的方法是。
(5)滤液中,需加入适量的试剂,这种试剂的名称是。
(6)在操作4中,需要进行蒸发,蒸发时需用到的仪器有铁架台(含铁圈)、酒精灯、玻璃棒、。
(7)若精盐的产率偏低,可能的原因是。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解粗盐时,加入的水量不足,粗盐没有完全溶解