现有一瓶标签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完成了如下实验: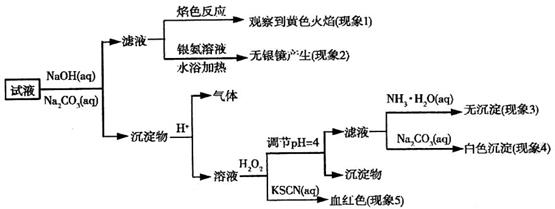
已知:控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。该同学得出的结论正确的是
| A.根据现象1可推出该试液中含有Na+ |
| B.根据现象2可推出该试液中并不含有葡萄糖酸根 |
| C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+ |
| D.根据现象5可推出该试液中一定含有Fe2+ |
下列离子方程式正确的是
A.用氢氧化钠溶液吸收二氧化氮:2OH-+2NO2===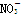 +NO↑+H2O +NO↑+H2O |
B.碳酸氢钠溶液与过量的澄清石灰水反应: +Ca2++2OH-===CaCO3↓+ +Ca2++2OH-===CaCO3↓+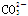 +2H2O +2H2O |
C.浓盐酸酸化的KMnO4溶液与H2O2反应: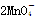 +6H++5H2O2===2Mn2++5O2↑+8H2O +6H++5H2O2===2Mn2++5O2↑+8H2O |
D.硫酸氢钠溶液与足量氢氧化钡溶液混合:H++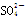 +Ba2++OH-===BaSO4↓+H2O +Ba2++OH-===BaSO4↓+H2O |
下列实验对应的结论不正确的是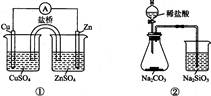

| A.①能组成Zn-Cu原电池 | B.②能证明非金属性Cl>C>Si |
C.③能说明2NO2 N2O4△H<0 N2O4△H<0 |
D.④中自色沉淀为BaSO4 |
下列日常生活中的现象与氧化还原反应无关的是
| A.铜铸塑像上出现铜绿[Cu2(OH)2CO3] | B.用石膏点豆腐 |
| C.不良商贩用硫黄熏蒸法制作“白豆芽” | D.自来水厂用氯气对水进行消毒 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,22.4 L NO与11.2 L O2充分反应后得到的气体分子数为NA |
| B.3.6 g重水中含有的中子数为2NA |
| C.一定条件下,6.4 g铜与过量的硫反应,转移电子数目为0.2NA |
| D.常温下,1 L 1 mol·L-1的CH3COOH溶液中,所含溶质分子数小于NA |
H2SO4和HNO3的浓度分别为4mol/L和2mol/L的混合液,取10mL加入过量的铁粉,若HNO3的还原产物为NO,则生成气体在标况下的总体积为
| A.0.224L | B.0.672L | C.0.112L | D.0.336L |