已知:2Fe2++Br2=2Fe3++2Br-,2Fe3++2I-=2Fe2++I2。向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。下列有关说法中,不正确的是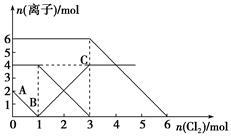
| A.还原性:I->Fe2+>Br- |
| B.原混合溶液中FeBr2的物质的量为6 mol |
| C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3 |
“茶倍健”牙膏中含有茶多酚,其中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中正确的是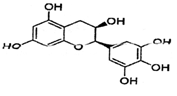
A.分子式为C15H12O7
B.EGC可在强碱的醇溶液中发生消去反应
C.1molEGC最多消耗6molNaOH
D.1molEGC可与4molBr2发生取代反应
有机物X完全燃烧的产物只有二氧化碳和水,元素组成分析发现,该物质中碳元素的质量分数为60.00%,氢元素的质量分数为13.33%,它的核磁共振氢谱有4组明显的吸收峰。下列关于有机物X的说法不正确的是
A.含有C、H、O三种元素B.相对分子质量为60
C.分子组成为C3H8O D.结构简式为CH3CHOHCH3
分子式为C4H10O并能与金属钠反应放出氢气的有机物(醚不能反应)有
| A.3种 | B.4种 | C.5种 | D.6种 |
乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是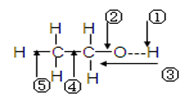
| A.和金属钠作用时,键②断裂 |
| B.和浓硫酸共热至170℃时,键①和⑤断裂 |
| C.和乙酸、浓硫酸共热时,键①断裂 |
| D.在铜催化下和氧气反应时,键①和②断裂 |
下列醇既能发生消去反应,又能被氧化为醛的是