下列指定反应的离子方程式正确的是
| A.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
| C.澄清石灰水中滴加少量NaHCO3: Ca2++ 2OH++2HCO3-= CaCO3↓+2H2O+ CO32- |
| D.向Mg(HCO3)2溶液中加入过量的 NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
下列说法正确的是
| A.0.18mol·L-1的醋酸加水稀释,c(H+)/c(OH-)减小 |
| B.体积相同、pH相同的醋酸和盐酸完全溶解等量的镁粉,后者用时少 |
| C.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大(不考虑温度变化) |
| D.V1LpH=11的NaOH溶液与V2LpH=3的HA溶液混合,若混合液显中性,则V1≤V2 |
利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如图所示的循环系统实现光分解水制氢(a、b、c、d均为惰性电极)。反应过程中所需的电能由太阳能光电池提供,反应体系中I2 和Fe3+ 等可循环使用。下列说法正确的是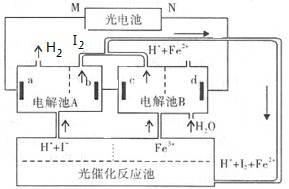
| A.电极M为光电池的正极 |
| B.d的电极反应式为2H2O + 4e- = 4H+ + O2↑ |
C.光催化反应池中反应的离子方程式为2Fe3++ 2I- 2Fe2+ + I2 2Fe2+ + I2 |
D.若循环系统处于稳定工作状态时,电解池A中流入和流出的HI浓度分别为a mol·L-1和b mol·L-1,光催化反应生成Fe3+ 的速率为c mol·min-1,则循环系统中溶液的流量为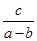 L·mol -1 L·mol -1 |
据下图判断,下列说法不正确的是
| A.(C6H10O5)n可表示淀粉或纤维素 |
| B.反应②化学方程式为C6H12O62C2H5OH+2CO2↑ |
| C.反应③得到的乙酸乙酯中含有乙醇和乙酸,可用饱和氢氧化钠溶液除去 |
| D.反应③和④都属于取代反应 |
已知:①Na3N+3H2O=3NaOH+NH3↑,②NaH+H2O=NaOH+H2↑。下列叙述正确的是
| A.离子半径:Na+>N3->H+ |
| B.反应①和②都是氧化还原反应 |
| C.反应②每生成1 mol H2,转移的电子数为NA |
| D.Na3N和NaH与盐酸反应都只生成一种盐 |
已知某物质X能发生如下转化:
下列有关上述转化关系中物质及其反应的叙述错误的是
A若X��N2或NH3(催化氧化),则A为硝酸
B若X为S 或H2S(完全燃烧),则A为硫酸
C若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y
D反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应