“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的副作用。下列化学反应,不符合绿色化学的是
| A.消除硫酸厂尾气排放:SO2+2NH3+H2O===(NH4)2SO3 |
| B.消除制硝酸工业尾气的氮氧化物污染:NO+NO2+2NaOH===2NaNO2+H2O |
| C.制CuSO4:Cu+2H2SO4(浓)===CuSO4+SO2↑+2H2O |
D.制CuSO4:2Cu+O2 2CuO ,CuO+H2SO4(稀)===CuSO4+H2O 2CuO ,CuO+H2SO4(稀)===CuSO4+H2O |
对下列事实的解释正确的是 ()
| A.浓硝酸通常保存在棕色的试剂瓶中,说明浓硝酸具有不稳定性 |
| B.浓硫酸具有吸水性,说明可用浓硫酸干燥氨气 |
| C.足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+ |
| D.常温下,可用铝制容器盛装浓硫酸,说明浓硫酸与铝不反应 |
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),反应结果并不改变的是 ( )
| A.Na和O2 | B.Cu和硝酸 | C.Cu和硫酸 | D.Al和NaOH |
用10mL的0.1mol/L BaCl2溶液恰好可使相同体积的硫酸铝、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是()
| A.3:2:2 | B.1:3:3 | C.2:3:6 | D.3:1:1 |
氮化铝(AlN)具有耐高温.抗冲击,导热性好等优良性质,被广泛应用于电子工业.陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3 + N2 + 3C 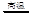 2AlN + 3CO下列叙述正确的是()
2AlN + 3CO下列叙述正确的是()
| A.在氮化铝的合成反应中,N2是还原剂,Al2O3氧化剂 |
| B.氮化铝是铝合金中的一种 |
| C.上述反应中每生成2molAlN,N失去6mol电子 |
| D.氮化铝中氮元素的化合价为-3 |
下列实验过程中出现的异常情况,其可能原因分析错误的是()
| 选项 |
异常情况 |
可能原因分析 |
| A |
蒸发结晶:蒸发皿破裂 |
将溶液蒸干或酒精灯灯芯碰到热的蒸发皿底部 |
| B |
分液:分液漏斗中的液体难以滴 下 |
没有打开分液漏斗活塞,或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐 |
| C |
萃取:液体静置不分层 |
加入萃取剂的量较多 |
| D |
蒸馏:冷凝管破裂 |
冷凝管没有通水或先加热后通水 |