今有如下三个热化学方程式:
①H2(g)+1/2O2(g) = H2O(g)ΔH=a kJ·mol-1 ②H2(g)+1/2O2(g) = H2O(l)ΔH=b kJ·mol-1
③2H2(g)+O2(g) = 2H2O(l) ΔH=c kJ·mol-1
关于它们的下列表述,正确的是
| A.它们都是吸热反应 | B.氢气的燃烧热为ΔH=a kJ·mol-1 |
| C.反应热的关系:a=b | D.反应热的关系:2b=c |
用氯气漂白过的石蜡(一种从石油分馏得到的固体),燃烧时会产生含氯元素的气体,这是由于石蜡在漂白时与氯气发生了()
| A.物理溶解 | B.加成反应 | C.取代反应 | D.加聚反应 |
某高分子化合物含有如下结构片段对此结构的分析正确的是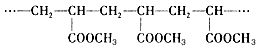
| A.它是加聚反应的产物 |
| B.合成它的小分子是CH3OH |
| C.合成它的小分子是CH2=CH2和HCOOCH3 |
| D.合成它的小分子是CH2=CHCOOCH3 |
下列对某些合成材料,如塑料制品废弃物的处理方法正确的是( )
| A.将废弃物混在垃圾中填埋在土壤里 |
| B.将废弃物焚烧 |
| C.将废弃物用化学方法加工成涂料或汽油 |
| D.将废弃物倾倒在海洋中 |
四氟乙烯的分子式为CF2==CF2,它的加聚反应的产物聚四氟乙烯可以作为不粘锅的内衬,其结构可表示为( )