可逆反应mA(g)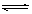 nB(g)+pC(s); △H=Q, 温度、压强的变化对正、逆反应速率的影响符合图中的两个图像,以下叙述正确的是
nB(g)+pC(s); △H=Q, 温度、压强的变化对正、逆反应速率的影响符合图中的两个图像,以下叙述正确的是
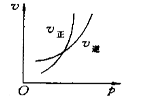
| A.m>n, Q>0 | B.m>n,Q<0 | C.m>n+p,Q>0 | D.m<n+p, Q <0 |
氢原子的3d和4s能级的能量高低是
| A.3d>4s | B.3d=4s |
| C.3d<4s | D.无3d,4s轨道,无所谓能量高低 |
有A、B和C三种主族元素,若A元素阴离子与B、C元素的阳离子具有相同的电子层结构,且B的阳离子半径大于C的阳离子半径,则这三种元素的原子序数大小次序是
A.B<C<AB.A<B<C
C.C<B<AD.B>C>A
超重元素的假说预言自然界中可存在原子序数为114号的稳定同位素 ,试根据原子结构理论和元素周期律预测正确的是
,试根据原子结构理论和元素周期律预测正确的是
A. 位于第七周期,第ⅣA族 位于第七周期,第ⅣA族 |
B.X是非金属元素 |
| C.XO2是酸性氧化物 | D.X元素的化合价有+2和+4 |
具有下列电子排布式的原子中,半径最大的是
| A.ls22s22p63s23p1 | B.1s22s22p3 |
| C.1s22s2sp2 | D.1s22s22p63s23p4 |
一个电子排布为1s22s22p63s23p1的元素最可能的价态是
| A.+1 | B.+2 | C.+3 | D.—1 |