现有Na2CO3和NaHCO3的混合物a克,下列实验方案不能测定混合物中Na2CO3质量分数的是
| A.与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| B.充分加热,得b克固体 |
| C.与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| D.与足量CaCl2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
下列说法正确的是
| A.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.升高温度能使化学反应速率增大,原因是增加了反应物分子中活化分子的百分数 |
| D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:Pb+ PbO2 + 2H2SO4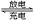 2PbSO4 + 2H2O根据此反应判断下列叙述中正确的是
2PbSO4 + 2H2O根据此反应判断下列叙述中正确的是
| A.放电时PbO2是电池的负极 |
| B.放电时,负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| C.放电时,溶液中的H+向正极区移动,正极区域的溶液的酸性增强 |
| D.充电时,该电池的正极接电源的负极 |
下列关于化学反应速率的说法正确的是
| A.化学反应速率是指单位时间内任何一种反应物物质的量的浓度的减少或任何一种生成物的物质的量的浓度的增加 |
| B.化学反应速率为1.0 mol·L-1·s-1,是指在1 s时某物质的浓度是1.0 mol·L-1 |
| C.化学反应速率可以衡量化学反应进行的快慢 |
| D.对于任何化学反应来说,反应速率越快,反应现象不一定越明显 |
下列有关电化学的装置完全正确的是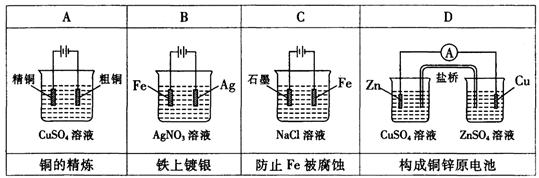
用惰性电极实现电解,下列说法正确的是
| A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变 |
| B.电解稀氢氧化钠溶液,要消耗OH-,故需加NaOH固体才能恢复到原溶液 |
| C.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1 |
| D.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2 |