酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的酸性K2Cr2C7水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧衍生物
| A.②④ | B.②③ | C.①③ | D.①④ |
反应C(s)+H2O(g)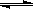 CO(g)+H2(g)在一可变容积的密闭容器内进行,达到平衡后,保持其他条件不变,下列条件的改变一定能使平衡移动的是
CO(g)+H2(g)在一可变容积的密闭容器内进行,达到平衡后,保持其他条件不变,下列条件的改变一定能使平衡移动的是
| A.增加C的质量 |
| B.保持体积不变,充入氦气使体系压强增大 |
| C.加入催化剂 |
| D.保持压强不变,充入氦气使容器体积增大 |
| 物质 |
X |
Y |
Z |
| 初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
| 平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
在一定条件下发生反应:2A(g)+2B(g)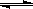 xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率V(D)=0.2mol·L-1·min-1,下列说法正确的是
xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率V(D)=0.2mol·L-1·min-1,下列说法正确的是
A.A和B的转化率均是20%
B.x =" 4"
C.平衡时A的物质的量为2.8mol
D.平衡时气体压强比原来减小
恒温条件下,对于可逆反应A(g)+ B(g)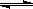 C(g)+ D(g),加入起始浓度相近的A和B,在达到平衡的过程中可能有三种情况,如下图所示。下列判断中正确的是
C(g)+ D(g),加入起始浓度相近的A和B,在达到平衡的过程中可能有三种情况,如下图所示。下列判断中正确的是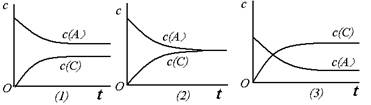
| A.⑴的K<1 | B.⑵的K≈1 | C.⑶的K>1 | D.以上三种可能全对 |
反应3A(g)+B(g)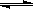 2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
A.v (A)="0.15" mol·L-1·s-1B.v (B)="0.3" mol·L-1·s-1
C.v (C)="0.5" mol·L-1·s-1D.v(D)="0.4" mol·L-1·s-1
在一定温度下,反应A2(g)+B2(g)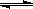 2AB(g)达到平衡的标志是(NA代表阿伏加德罗常数)
2AB(g)达到平衡的标志是(NA代表阿伏加德罗常数)
| A.单位时间生成NA的A2同时生成NA的AB |
| B.容器内的总压不随时间变化 |
| C.单位时间生成2NA的AB同时生成NA的B2 |
| D.单位时间生成NA的A2同时生成NA的B2 |