高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为
2Fe(OH)3 + 3KClO + 4KOH ="=" 2K2FeO4 + 3KCl + 5H2O,下列说法正确的是
| A.制备高铁酸钾用ClO−做还原剂 |
| B.制备高铁酸钾时1 mol Fe(OH)3得到3 mol 电子 |
| C.高铁酸钾中铁的化合价为+7 |
| D.用高铁酸钾处理水时,其还原产物能水解产生具有强吸附能力的胶体 |
对于可逆反应 2AB3(g) 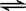 A2(g) + 3B2(g),△H>0;下列图像正确的是
A2(g) + 3B2(g),△H>0;下列图像正确的是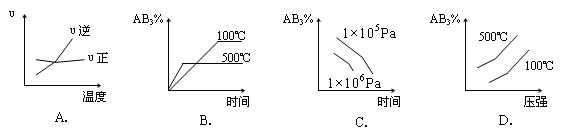
在一定温度不同压强(P1<P2)下,可逆反应2X(g) 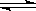 2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是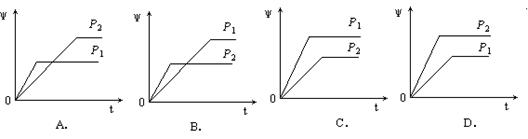
在可逆反应中,改变下列条件一定能加 快反应速率的是
快反应速率的是
| A.增大反应物的量 | B.升高温度 | C.增大压强 | D.使用催化剂 |
某温度下,在容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为6mol、3mol和6mol。保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,可使平衡右移的是
2C(g)达到平衡时,A、B和C的物质的量分别为6mol、3mol和6mol。保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,可使平衡右移的是
A.均减半 B.均加倍 C.均增加2mol D.均减少2mol
将固体NH4I置于密闭容器中,在某温度下发生下列反应: NH4I(s)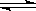 NH3(g)+HI(g),2HI(g)
NH3(g)+HI(g),2HI(g) 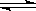 H2(g)+I2(g)。当反应达到平衡时,c(H2
H2(g)+I2(g)。当反应达到平衡时,c(H2 )=0.5 mol·L-1,c(HI)=4 mol·L-1,则NH3的浓度为
)=0.5 mol·L-1,c(HI)=4 mol·L-1,则NH3的浓度为
| A.3.5 mol·L-1 | B.4 mol·L-1 | C.4.5 mol·L-1 | D.5 mol·L-1 |