在pH=1的溶液中,能大量共存的一组离子是
| A.Al3+、NH4+、Br-、Cl- | B.Mg2+、Ca2+、HCO3-、NO3- |
| C.K+、MnO4-、S2-、SO42- | D.Na+、K+、SiO32-、Cl- |
下列各分子中,所有原子都满足最外层为8电子结构的是
| A.H2O | B.BF3 | C.CCl4 | D.PCl5 |
决定原子种类的因素是
| A.电子数 | B.质子数 | C.质子数和中子数 | D.质子数和电子数 |
体积相同、C(H+)相同的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是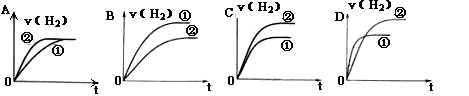
A. B. C. D.
体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2 2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
近年来,科学家研制了一种新型的乙醇电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是
| A.乙醇在电池的负极上参加反应 |
| B.1mol CH3CH2OH被氧化转移6mol e- |
| C.随着反应的进行,正极附近的酸性减弱 |
| D.电池正极的正极反应为4H++O2+4e-=2H2O |