下列热化学方程式或离子方程式正确的是
| A.已知H2的标准燃烧热ΔH=-285.8 kJ·mol-1,则用热化学方程式可表示为: H2(g)+1/2O2(g)===H2O(g)ΔH=-285.8 kJ·mol-1 |
| B.NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O===Fe(OH)2↓+2HClO |
C.NH4HSO3溶液与足量NaOH溶液共热:NH4++H++2OH-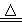 NH3↑+2H2O NH3↑+2H2O |
| D.用足量KMnO4溶液吸收SO2气体:2MnO4-+5SO2+2H2O===2Mn2++5SO42-+4H+ |