仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
…… |
| C2H2 |
C2H4 |
C2H6 |
C3H4 |
C3H6 |
C3H8 |
C4H6 |
C4H8 |
C4H10 |
…… |
A.C6H12 B.C6H14 C.C7H12 D.C7H14
提出元素周期律并绘制了第一个元素周期表的科学家是
| A.戴维 | B.阿伏加德罗 | C.门捷列夫 | D.道尔顿 |
下列四个有机反应中,其中一个反应与其它三个反应的反应类型不同的是
下列物质所属的类别及其所含官能团的对应关系有错误的是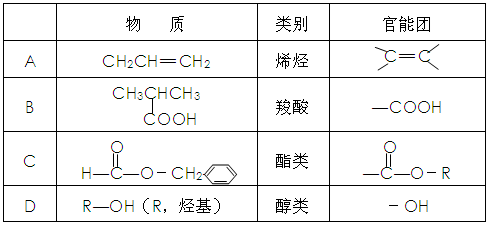
某有机物的结构简式为 ,下列对其化学性质的判断中不正确的是
,下列对其化学性质的判断中不正确的是
| A.能被银氨溶液氧化 |
| B.能使KMnO4酸性溶液褪色 |
| C.1mol该有机物只能与1mol Br2发生加成反应 |
| D.1mol该有机物只能与1mol H2发生加成反应 |
1mol某烃完全燃烧,可得到3mol CO2,在一定条件下,1mol该烃能与2mol H2发生加成反应,这种烃是
CO2,在一定条件下,1mol该烃能与2mol H2发生加成反应,这种烃是
| A.C2H6 | B.C2H4 | C.C2H2 | D.C3H4 |