如图为课本中的插图,下列操作不合理的是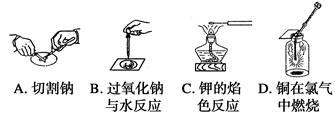
下列金属冶炼的反应原理,错误的是
A.2NaCl(熔融) 2Na + Cl2↑ 2Na + Cl2↑ |
B.Al2O3 + 3H2 2Al + 3H2O 2Al + 3H2O |
C.Fe2O3+ 3CO  2 Fe + 3CO2 2 Fe + 3CO2 |
D.MgCl2 Mg + Cl2↑ Mg + Cl2↑ |
关于Na2O和Na2O2的叙述正确的是
| A.都是白色固体 | B.都是碱性氧化物 |
| C.都能和水反应形成强碱溶液 | D.都具有强氧化性 |
由海水提取金属镁,主要有以下步骤:①在一定条件下脱水干燥;②加石灰乳;③加盐酸;④过滤;⑤蒸发结晶;⑥电解。其先后顺序正确的是
| A.②④⑤③①⑥ | B.③②④①⑤⑥ |
| C.③④②⑤①⑥ | D.②④③⑤①⑥ |
下列溶液与20mL 1 mol·L—1 NaNO3溶液中NO3— 物质的量浓度相等的是
| A.10 mL 1 mol·L—1 Mg(NO3)2溶液 |
| B.5 mL 0.8 mol·L—1 Al(NO3)3溶液 |
| C.10 mL 2 mol·L—1 AgNO3溶液 |
| D.10 mL 0.5 mol·L—1 Cu(NO3)2溶液 |
下列四种物质的溶液,其中一种与其它三种能发生离子反应,这种物质是
| A.H2SO4 | B.KOH | C.BaCl2 | D.Na2CO3 |