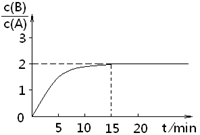
某温度下在2L密闭容器中加人一定量A,发生以下化学反应:2A(g) 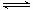 B(g)+C(g);ΔH =-48.25kJ/mol。反应过程中B、A的浓度比与时间t有右图所示关系,若测得第15min时c(B)=1.6mol/L,下列结论正确的是
B(g)+C(g);ΔH =-48.25kJ/mol。反应过程中B、A的浓度比与时间t有右图所示关系,若测得第15min时c(B)=1.6mol/L,下列结论正确的是
A.该温度下此反应的平衡常数为3.2
B.A的初始物质的量为4mol
C.反应到达平衡时,放出的热量是193kJ
D.反应达平衡时,A的转化率为80%
铁和氧化铁的混合物共x mol,加盐酸后固体全部溶解,共收集到ymol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则反应后溶液中Fe元素质量为
| A.56(3x+y)g | B.56(3x-y) g |
| C.28(3x+y)g | D.28(3x-y)g |
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
| A.加入KSCN溶液一定不变红色 | B.溶液中一定含Cu2+ |
| C.溶液中一定含Fe2+ | D.剩余固体中一定含铜 |
将5.4 g Al投入到200.0 mL 1.00mol/L的某溶液中有氢气产生,充分反应后没有金属剩余,该溶液可能为
| A.HNO3溶液 | B.HCl溶液 | C.H2SO4溶液 | D.NaOH溶液 |
下列实验方案中,能测定Na2CO3和NaHCO3混合物中NaHCO3质量分数的是
①取a克混合物充分加热,减重b克
②取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
③取a克混合物与足量稀硫 酸充分反应,逸出气体先用浓硫酸干燥再用碱石灰吸收,碱石灰增重b克
酸充分反应,逸出气体先用浓硫酸干燥再用碱石灰吸收,碱石灰增重b克
④取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
| A.只有①②④ | B.①②③④ | C.只有①③④ | D.只有①②③ |
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合下图。
则甲和X(要求甲和X互换后也能符合要求)不可能是
①Na2CO3溶液和稀盐酸②Cl2和Fe③C和O2
④SO2和NaOH溶液⑤AlCl3溶液和NaOH溶液
| A.②③④均可以 | B.③④⑤均可以 |
| C.①③⑤均可以 | D.①③④均可以 |