已知某粗盐样品含有Na2SO4、MgCl2、CaCl2等杂质。实验室提纯流程如下:
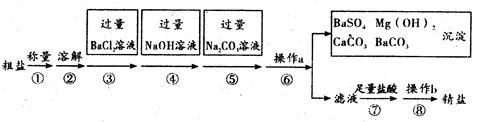
(1)操作a的名称为 ,在操作b中玻璃棒的作用是 。
(2)进行步骤③后,判断BaCl2过量的方法是 (写出步骤、现象)。
(3)步骤⑤的目的是 ,步骤⑦中能用稀硫酸代替稀盐酸吗? 。
甲、乙、丙是由短周期元素形成的常见单质,丙在常温下为无色气体,且乙、丙两元素同主族,其余均为常见化合物,它们在一定条件下有如下转化关系(反应中生成的水已略去)。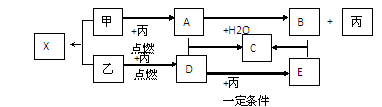
⑴C的化学式是;B中所含化学键的类型。
⑵A+D→C的反应属于下列何种反应类型(填字母)。
| A.化合反应 | B.氧化还原反应 | C.非氧化还原反应 | D.离子反应 |
⑶写出甲与H2O反应的化学方程式:。
⑷请用右图装置证明A和H2O反应是放热反应并有丙生成。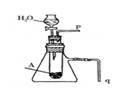
简述合理的实验操作方法:
①。
②。
为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如下: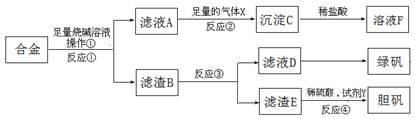
请回答:
(1)操作①的名称是。
(2)写出反应①的化学方程式,
反应②的离子反应方程式。
(3)设计实验方案,检测滤液D中含有的金属离子(试剂自选)。
(4)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无色液体,反应④的总化学方程式是。
(5)乙同学在甲同学方案的基础上提出用滤渣B来制备 FeCl3?6H2O晶体,在滤渣中滴加盐酸时,发现反应速率比同浓度盐酸与纯铁粉反应要快,其原因是,将所得氯化铁溶液用加热浓缩、降温结晶法制得FeCl3?6H2O晶体,而不用直接蒸发结晶的方法来制得晶体的理由是 。
那格列奈是一种新型的餐时血糖调节剂,适用于2型糖尿病。其合成路线如下: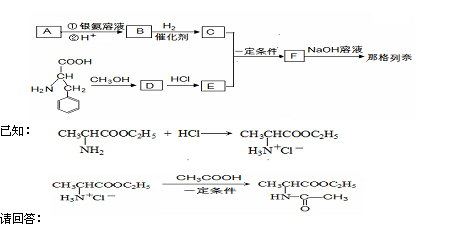
(1)有机物A蒸气密度是相同状态下氢气密度的74倍,A分子中碳元素的质量分数是氢元
素质量分数的10倍,A的1个分子中含有1个氧原子, A中含氧官能团的名称为;
A的分子式为。
(2)A的结构满足以下条件:
① 含有苯环,苯环上有两个取代基
② 苯环上的一溴取代物只有两种
③ 取代基上有三种不同的氢
写出A的结构简式:____________________________________________________________
(3)写出流程中制取D的化学方程式;
_____________________________________________________________________________
(4)由F制取那格列奈的反应类型是____________________
(5)(5)1 mol B与3 mol H2加成得到C,写出由C和E制取F的化学方程式:
___________________________________________________________________________、
A、B、C、D、E均为有机化合物,它们之间的关系如图所示(提示:RCH=CHR’在酸性高锰酸钾溶液中反应生成RCOOH和R’COOH,其中R和R’为烷基)。
回答下列问题:
(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其余为氧元素,则A的分子式为_▲;B的结构简式是_▲
(2)已知B与NaHCO3溶液完全反应,其物质的量之比为1:2,则在浓硫酸的催化下,B与足量的C2H5OH发生反应的化学方程式是▲,反应类型为_▲:
(3)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是▲
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有▲种,其相应的结构简式是▲
(1)苏合香醇可以用作食用香精,其结构简式如图所示。
苏合香醇的分子式为,它不能发生的有机反应类型有(填数字序号)。
①取代反应 ②加成反应 ③氧化反应 ④加聚反应
(2)苏合香醇属于酚类有机物的同分异构体共有种
(3) 的同分异构体有多种,满足下列条件的共有种。
的同分异构体有多种,满足下列条件的共有种。
① 苯环上只有两个取代基
② 1 mol 与足量的NaHCO3溶液反应生成2 mol CO2气体