某化学小组对铁的冶炼、铁的锈蚀与防护进行以下实验探究.
(1)该小组设计如图1研究铁的冶炼.

①实验时,应先注水片刻后再加热的目的是 .
②硬质玻璃管中发生反应的化学方程式是 .
(2)该小组又设计如图2装置,将反应所得铁粉置于锥形瓶底部,塞紧瓶塞,滴加适量食盐水,开始 测量容器内压强的变化.压强与时间变化关系如图3所示:
①实验中食盐的作用是 .
②锥形瓶内压强下降的原因是 .
③生产、生活中铁制品的常见防锈方法有 (举一例).
合金在生活中应用十分广泛。已知某合金粉末除含金属铝外,还含有铁、铜中的一种或两种。小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动。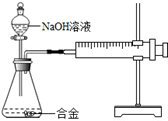
【提出问题】难道NaOH溶液也能与某些金属发生化学反应吗?
【查阅资料】
(1)铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应。
(2)铝与氢氧化钠溶液反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑(其中,NaAlO2溶于水,溶液呈无色)
【进行猜想】猜想1:该合金粉末中除铝外,还含有铁;
猜想2:该合金粉末中除铝外,还含有 ;
猜想3:该合金粉末中除铝外,还含有铁、铜。
【实验探究】下列实验(见下表)仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液。
实验记录:
| 实验步骤 |
实验现象 |
结论 |
| ①取一定量的合金粉末,加过量的,充分反应后过滤,滤渣备用 |
粉末部分溶解,并有无色气体放出,形成无色溶液 |
合金中一定含有 |
| ②取步骤①所得滤渣,加过量,充分反应 |
滤渣部分溶解,并有无色气体放出,溶液呈浅绿色 |
合金中一定含有 |
【得出结论】猜想3成立。
【拓展】下列可用于小明验证铝、铁、铜三种金属的活动性强弱的一组药品是
A.Fe、Cu、Al(NO3)3溶液 B.Al、Fe、Cu、稀盐酸
C.Al 、Cu、FeSO4溶液 D.Cu、Al(NO3)3溶液、FeSO4溶液
铁质水龙头长期使用容易生锈,小明从自家水龙头上取下一些铁锈样品,用图甲所示的装置进行实验。 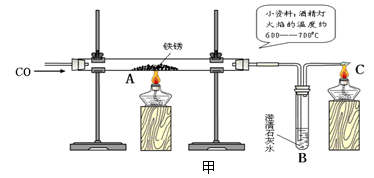
(1)B处澄清石灰水变浑浊,反应方程式为,C处酒精灯的作用是
(2)实验结束,小明将所得的黑色固体物质放入足量的稀硫酸中,发现没有气泡,这说明生成物中(有或没有)铁。
为解释这个现象,小明查阅下列资料:
Ⅰ.已知铁的氧化物有FeO、Fe3O4、Fe2O3,,在一定条件下,均能逐步失去其中的氧,最终被还原为铁。
Ⅱ.某炼铁厂对氧化铁和一氧化碳进行热反应分析,获得相关数据并绘制成下图。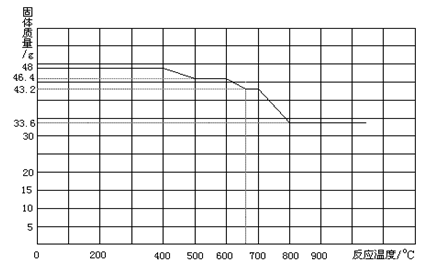
通过分析资料确定:
①700℃时氧化铁和一氧化碳进行反应的产物是(填FeO或Fe3O4或Fe).
②小明实验失败的主要原因是。
(1)目前世界上一半以上的铜用于电力和电信工业,是因为铜具有(填字母)
| A.导热性 | B.延展性 | C.导电性 | D.金属光泽 |
(2)我国第四套人民币的硬币从1999年开始发行,一元为钢芯镀镍(Ni ),五角币为钢芯镀铜合金,一角币为铝合金或不锈钢。在选择铸造硬币的材料时需要考虑的因素是有(填一条即可)。
①镍能与盐酸或稀硫酸反应,生成可溶于水的正二价镍的化合物,并放出氢气。其反应没有铁与酸反应剧烈。镍与盐酸反应的化学方程式为.
②用镍片、硫酸亚铁溶液和溶液做实验也能判断Ni 、Fe、Cu的金属活动性顺序。三种金属的活动性顺序为。
(3)若将一定质量的Zn放入CuCl2和MgCl2的混合溶液中,充分反应后过滤,所得滤液中一定含有的溶质是。
(4)活动课上小明将一枚五角币放在酒精灯火焰上加热片刻,发现表面变黑。
【假设与预测】假设Ⅰ:五角币加热变黑,是因为酒精灯内焰的黑烟附着在五角币的镀铜上;
假设Ⅱ:五角币加热变黑,是因为五角币上的镀铜与 ______发生了化学反应。
【实验与事实】
实验一: 用洁净的干布擦一擦五角币上的黑色物质,黑色物质不易被擦去;再另取一枚五角币放在石棉网上,用酒精灯加热片刻,五角币也变黑。
实验二:取一块铜片放入小试管中并塞上橡皮塞,然后用酒精灯加热直至试管中铜片变黑;再将铜片反转到另一面,加热片刻,铜片不再变黑。
【解释与结论】上述实验一和实验二证实,假设 __ ___不成立。
【表达与交流】铜片在空气中加热,发生的化学反应方程式为___ ___。
6月5日是“世界环境日”,2013年中国主题为“同呼吸共奋斗”。
(1)化石燃料是不可再生能源,包括煤、 和天然气等。
(2)下列不属于空气污染物的是 。
| A.二氧化氮 | B.二氧化硫 | C.PM2.5 | D.氧气 |
(3)二氧化碳是一种温室气体。某化学兴趣小组进行如下组合实验,对二氧化碳的性质进行验证。
当打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中。E处紫色石蕊溶液变成红色,F处澄清石灰水变浑浊。
①A中发生反应的化学方程式为 。
②B中白磷能够燃烧的原因是 。
③G烧杯中 (填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的物理性质是 ,具有的化学性质是 。
④E处使紫色石蕊变成红色的物质是 ;写出F处发生变化的化学方程式 。
某化学兴趣小组的同学对一瓶久置的熟石灰粉末的组成进行实验探究,请你一起参与他们的探究活动。
[提出问题]这瓶熟石灰粉末是否已经变质生成了CaCO3?
[进行猜想]猜想一: 。
猜想二:熟石灰部分变成了CaCO3。
猜想三:熟石灰没有变质。
[设计实验]该小组同学对猜想一设计了下列探究方案,请你帮助他们完成下表中相关实验内容。
| 实验步骤 |
实验现象 |
实验结论 |
| ①取样,加适量水,搅拌,过滤 ②取少量滤液于试管中,滴入酚酞试液 ③取少量滤渣于试管中,加入盐酸 |
②无明显变化。 ③。 |
猜想一成立 |
[反思与应用]①要证明猜想二成立,可参照上述实验方案进行探究,在步骤②中产生的实验现象是。
②熟石灰变质的化学反应方程式为,因此实验室中应保存。
[数据处理]将10g已经全部变质的熟石灰粉末(即CaCO3)放入烧杯中,加入一定量的稀盐酸,恰好完全反应,产生气体,完全反应后所得溶液质量为55.6g。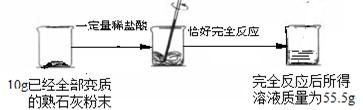
计算:①生成气体的质量为g ;参与反应的HCl的质量为g;
②反应前稀盐酸中溶质的质量分数。(写出计算过程,结果精确到0.1%)