用固体NaCl配制100g质量分数为15%的NaCl溶液.
(1)该实验除烧杯、量筒、胶头滴管和细口瓶外,还必须用到的玻璃仪器是 .
(2)实验中应选用规格为 (填“50”、“100”或“200”)mL的量筒.
(3)称量NaCl时,若天平指针偏左,应进行的操作是 .
(4)下列操作一定会导致NaCl质量分数偏低的是 (填序号).
①砝码和氯化钠放错托盘
②使用了生锈的砝码
③量水时仰视凹液面最低处读数
④装瓶时溶液洒落.
“学做营养师,我来配食谱。”我们来帮小明同学完成下列食谱。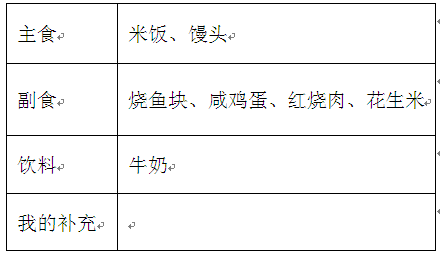
除了水和无机盐之外,上表食谱中,含有的营养素主要有___________________等(写两种);我认为小明列出的食谱中还缺少一种人体所必需的营养素____________,“我的补充”是_________(填写获取该营养素的一种食物名称)。
化学与我们生活密切相关,日常生活中的化学知识有很多。想想看,生活中常用的下列物质分别含有什么化学成分(填化学式):(1)干冰常用于人工降雨。干冰中的“冰”是指;(2)天然气是常用的气体燃料,天然气中的“气”是指;(3)纯碱是生活中常用的洗涤剂,纯碱中的“碱”是指;(4)碘酒是常用的皮肤消毒剂,碘酒中的“碘”是指。
通过一年的化学学习,应该知道有多种途径可以制取氧气。如:
| A.电解水 | B.分离空气 |
| C.加热高锰酸钾 | D.分解过氧化氢 |
E.
(1)相信你在E处还可以写出另一种制取氧气的方法;
(2)若用右图装置加热高锰酸钾制取氧气: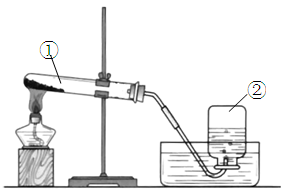
写出标号仪器的名称 ①②;
实验结束,停止加热时要先把导管移出水面,其理由是,此时发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是;
(3)若分解过氧化氢制取氧气,供选用的装置如下:
要得到平稳的氧气流,应选用的发生装置是(选填“甲”或“乙”);若用丙装置干燥生成的氧气,丙中盛放的液体试剂是,气体应从(选填“a”或“b”)端导入。
结合以下实验室制取气体的常用装置回答问题:
(1)写出标号仪器的名称:①;②。
(2)实验室用过氧化氢溶液与二氧化锰固体混合制取氧气时,应选用的发生装置是(填序号,下同),收集装置是,反应的化学方程式为。
(3)能用C装置收集的气体,必须具备的性质是。
(4)实验室选用A装置用高锰酸钾制取氧气,反应方程式为_____________________,用此方法制氧气时,试管口放一团棉花的作用是_________________________________。
实验室常用下列装置研究气体的制取和性质,根据所学知识回答下列问题。
(1) 写出实验室制取氧气的一个化学方程式。利用该反应制取氧气,发生装置应选(填序号,下同)。
(2) 一氧化氮气体难溶于水,在空气中容易发生下列反应2NO+O2==2NO2,则收集一氧化氮气体时不能用的装置是(填序号)。
(3) 按图F作细铁丝在氧气中燃烧的实验,其相关的化学方程式是。
(4) 实验室里将制得的二氧化碳气体通入澄清石灰水中,始终未出现浑浊现象,可能的原因是。