常温下,某无色透明的溶液中,下列各组离子能够大量共存的是
| A.H+、Na+、Cl-、CO32- | B.Ba2+、Na+、SO42-、Cl- |
| C.MnO4-、K+、I-、H+ | D.Mg2+、Cl-、NO3-、H+ |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。
其电池反应为:2CH3OH + 3O2 + 4OH— 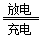 2CO32— + 6H2O,则下列说法错误的是()
2CO32— + 6H2O,则下列说法错误的是()
| A.放电时CH3OH参与反应的电极为正极 |
| B.充电时电解质溶液的C(OH-)逐渐增大 |
| C.放电时负极的电极反应为:CH3OH+8OH--6e-→ CO32— + 6H2O |
| D.充电时每生成1 mol CH3OH转移6 mol电子 |
已知 (1) H2(g)+1/2O2(g)=H2O(g)△H1=a kJ/mol
(2)2H2(g)+O2(g)=2H2O(g)△H2=b kJ/mol
(3)H2(g)+1/2O2(g)=H2O(l)△H3=c kJ/mol
(4)2H2(g)+O2(g)=2H2O(l)△H4=d kJ/mol
下列关系式中正确的是()
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
对于反应2SO2(g)+O2(g)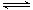 2SO3(g),能增大正反应速率的措施是()
2SO3(g),能增大正反应速率的措施是()
| A.移去部分SO3 | B.增大容器的体积 |
| C.通入大量O2 | D.升高体系温度 |
在一定温度下的定容密闭容器中,当下列物理量不再变化时,不能表明反应:
A(固)+2B(气)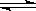 C(气)+D(气)已达平衡的是()
C(气)+D(气)已达平衡的是()
| A.混合气体的压强 | B.混合气体的密度 |
| C.B的物质的量浓度 | D.混合气体的平均相对分子质量 |
下列说法不正确的是()
| A.铁表面镀锌,铁作阳极 |
| B.船底镶锌块,锌作负极,以防船体被腐蚀 |
C.钢铁吸氧腐蚀的正极反应: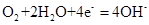 |
D.工业上电解饱和食盐水的阴极反应: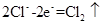 |